题目内容
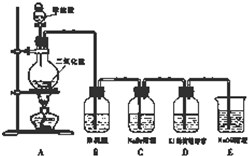 某校研究性学习小组设计实验,制取氯气以探究Cl2、Br2、I2的氧化性强弱(制取氯气的化学方程式为:MnO2+4HCl(浓)
某校研究性学习小组设计实验,制取氯气以探究Cl2、Br2、I2的氧化性强弱(制取氯气的化学方程式为:MnO2+4HCl(浓) | △ |
. |
【实验探究】D装置中溶液变
【实验讨论】有些同学对上述实验装置持有不同看法:
甲同学认为:B装置是多余的. 乙同学认为:B装置是必须的.
你认为
考点:氯气的实验室制法,氯、溴、碘的性质实验
专题:实验题
分析:氯气氧化性强于碘,能够与碘化钾反应生成单质碘,碘与淀粉变蓝色;
浓硫酸的具有吸水性,常用作干燥剂,图中B浓硫酸的作用干燥氯气,而氯气与溴化钾、碘化钾反应都是在水溶液中反应,氯气是否干燥对反应不会产生影响.
浓硫酸的具有吸水性,常用作干燥剂,图中B浓硫酸的作用干燥氯气,而氯气与溴化钾、碘化钾反应都是在水溶液中反应,氯气是否干燥对反应不会产生影响.
解答:
解:氯气氧化性强于碘,能够与碘化钾反应生成单质碘,碘与淀粉变蓝色;
图中B浓硫酸的作用干燥氯气,而氯气与溴化钾、碘化钾反应都是在水溶液中反应,氯气是否干燥对反应不会产生影响,所以B装置是多余的;
故答案为:蓝色;甲.
图中B浓硫酸的作用干燥氯气,而氯气与溴化钾、碘化钾反应都是在水溶液中反应,氯气是否干燥对反应不会产生影响,所以B装置是多余的;
故答案为:蓝色;甲.
点评:本题为实验题,考查了氯气的性质和实验评估,题目难度不大,熟悉氯气的性质是解题关键,注意反应发生的条件.

练习册系列答案
相关题目
如图是空气氧化Fe2+转化为Fe3+过程中的实验结果,下列有关说法正确的是( )


| A、使用5% H2SO4氧化效果一定比5% HCl好 |
| B、实验过程最佳氧化条件一定是80℃、5%HCl氧化4小时左右 |
| C、50℃时,图中H2SO4比HCl中氢离子浓度大,所以氧化率高 |
| D、该反应的离子方程式为:4Fe2++O2+4H+═4Fe3++2H2O |
下列化学反应中反应速率最大的是( )
| A、25℃时1g镁投入100ml 0.5mol/L盐酸溶液中 |
| B、25℃时1g镁投入200ml 0.5mol/L盐酸溶液中 |
| C、25℃时1g镁投入50ml 1mol/L盐酸溶液中 |
| D、50℃时1g镁投入10ml 1mol/L盐酸溶液中 |
在FeCl3、CuCl2混合溶液中,加入过量的铁屑,反应完全后将固体滤出,下列说法正确的是( )
| A、若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+? |
| B、若滤出的固体中含有铁和铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+和Fe3+ |
| C、若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,可能含有Cu2+和Fe3+? |
| D、若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe3+和Fe2+,一定不含Cu2+ |
一定的固体硝酸银置于一容积不变的2L密闭容器中,在一定条件下发生如下反应2AgNO3(s)?2Ag(s)+2NO2(g)+O2(g),2NO2(g)?N2O4(g).2min末,测得固体减重6.2g,且C(NO2)=0.04mol/L,则下列说法正确的是( )
| A、2min后容器内c(N2O4)=0.04mol/L |
| B、2min内v(O2)=0.0125mol/L?min |
| C、混合气体的平均密度为3.1g/L |
| D、混合气体中NO2的体积分数为0.11 |
