题目内容
20.下列叙述正确的是( )| A. | 离子化合物中只存在离子键 | |
| B. | 任何物质中都存在化学键 | |
| C. | 金属氧化物一定是碱性氧化物,非金属氧化物可能不是酸性氧化物 | |
| D. | 仅由非金属元素组成的化合物中可能含离子键,但仅由两个非金属原子构成的微粒不含离子键 |
分析 A.离子化合物中可能含有共价键;
B.单原子分子中没有化学键;
C.金属氧化物可能是两性氧化物或酸性氧化物;
D.铵盐由非金属元素组成,为离子化合物.
解答 解:A.离子化合物中可能含有共价键,如:氢氧化钠中氢原子和氧原子之间存在共价键,故A错误;
B.单原子分子中没有化学键,如稀有气体是单原子分子,不存在化学键,故B错误;
C.金属氧化物可能是两性氧化物或酸性氧化物,如氧化铝属于两性氧化物,所以金属氧化物不一定是碱性氧化物,非金属氧化物可能不是酸性氧化物,如CO是不成盐氧化物,故C错误;
D.铵盐由非金属元素组成,为离子化合物,含有离子键,仅由两个非金属原子构成的微粒不含离子键,故D正确.
故选D.
点评 本题考查了物质与化学键的关系,难度不大,易错选项是B,注意:不是所有物质都含化学键,如稀有气体中不存在化学键,只存在分子间作用力.

练习册系列答案
相关题目
8.下列液体温度均处在25℃,有关叙述正确的是( )
| A. | 某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 | |
| B. | pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 | |
| C. | 将1 L 0.1 mol•L-1的Ba(OH)2溶液稀释为2 L,pH=12 | |
| D. | pH=8的NaOH溶液稀释100倍,其pH=6 |
5.向以下四种溶液中分别持续通入CO2,最终得到沉淀的一组是( )
①BaCl2
②Ca(OH)2
③Na2SiO3
④Na[Al(OH)4].
①BaCl2
②Ca(OH)2
③Na2SiO3
④Na[Al(OH)4].
| A. | ①③④ | B. | ②③④ | C. | ③④ | D. | ①②③ |
12.下列元素中,原子半径最大的是( )
| A. | 锂 | B. | 钠 | C. | 氟 | D. | 氯 |
9.与CO32-不是等电子体的是( )
| A. | SO3 | B. | BF3 | C. | NO3- | D. | PCl3 |
10.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 强酸性溶液:Mg2+、K+、SO42-、NO3- | |
| B. | 使酚酞变红色的溶液:Na+、Cu2+、HCO3-、NO3- | |
| C. | 0.1mol•L-1AgNO3溶液:H+、K+、SO42-、I- | |
| D. | 0.1mol•L-lNaAlO2溶液:H+、Na+、Cl-、SO42- |
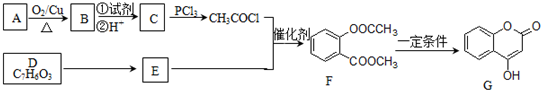


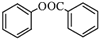 )的合成路线流程图(无机原料任用).
)的合成路线流程图(无机原料任用).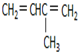 2-甲基-1,3-丁二烯;
2-甲基-1,3-丁二烯;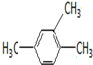 1,2,4-三甲基苯;
1,2,4-三甲基苯;