题目内容
7.在1.01×105Pa、120℃时,1LA、B两种烷烃组成的混合气体,在足量O2中充分燃烧后,得到同温同压下2.5LCO2和3.5L水蒸气,且A分子中比B少2个碳原子,试确定A和B的分子式及体积比A为甲烷、B为丙烷时,二者体积分别为0.25L、0.75L;当A为乙烷、B为丁烷时,二者体积分别为0.75L、0.25L.分析 根据相同条件下气体体积之比等于物质的量之比,由混合气体1L充分燃烧后得到同温同压下2.5LCO2和3.5L水蒸气,可知混合气体的平均分子式为C2.5H7,碳原子数小于2.5的烷烃有甲烷和乙烷,则另一种对应烷烃为丙烷和丁烷,结合平均分子式计算出二者的体积.
解答 解:同条件下气体体积之比等于物质的量之比,由混合气体1L充分燃烧后得到同温同压下2.5LCO2和3.5L水蒸气,可知混合气体的平均分子式为C2.5H7,
烷烃中碳原子数小于2.5的有甲烷和乙烷,
当一种烷烃为甲烷时,另一种烷烃为丙烷,设甲烷体积为x,乙烷体积为y,则$\frac{x+3y}{x+y}$=2.5,整理可得:x+y=1:3,则混合气体中含有甲烷体积为:1L×$\frac{1}{4}$=0.25L,含有丙烷体积为0.75L;
但一种烷烃为乙烷时,另一种烷烃为丁烷,设乙烷体积为x、丁烷体积为y,则$\frac{2x+4y}{x+y}$=2.5,整理可得:x+y=3:1,则混合气体中含有乙烷的体积为:1L×$\frac{3}{4}$=0.75L,含有丁烷的体积为0.25L,
故答案为:A为甲烷、B为丙烷时,二者体积分别为0.25L、0.75L;当A为乙烷、B为丁烷时,二者体积分别为0.75L、0.25L.
点评 本题考查了混合物反应的计算、有机物分子式的确定,题目难度中等,明确平均分子式的含义为解答关键,注意掌握平均值法、讨论法在化学计算中的应用方法.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
17.下列除杂方法正确的是( )
①除去乙烷中少量乙烯:通入足量H2,加入催化剂反应
②除去乙酸乙酯中的少量的乙酸:用足量饱和碳酸钠溶液洗涤,分液
③除去苯中少量的苯酚:滴入足量溴水,过滤
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏
⑤除去苯中少量的甲苯:先加足量酸性KMnO4溶液振荡后加足量的NaOH溶液,分液.
①除去乙烷中少量乙烯:通入足量H2,加入催化剂反应
②除去乙酸乙酯中的少量的乙酸:用足量饱和碳酸钠溶液洗涤,分液
③除去苯中少量的苯酚:滴入足量溴水,过滤
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏
⑤除去苯中少量的甲苯:先加足量酸性KMnO4溶液振荡后加足量的NaOH溶液,分液.
| A. | ①②③ | B. | ③④⑤ | C. | ②④⑤ | D. | ②③④ |
18.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 常温常压下,11.2L氯气所含的原子数目为NA | |
| B. | 标准状况下,1.12LO2和1.12 L CO2均含有0.1NA氧原子 | |
| C. | 标准状况下,22.4L空气含有NA个单质分子 | |
| D. | 标准状况下,22.4LH2O含有NA个水分子 |
7.(1)已知:
①2H2(g)+O2(g)=2H2O(l)△H1=-571.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ•mol-1
③CO(g)+2H2(g)?CH3OH(g)△H3=-90.8kJ•mol-1
计算甲醇蒸气的燃烧热△H=-763.8kJ•mol-1
(2)在某温度下,发生可逆反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.0kJ.mol-1
①向某容器中充入1.0molH2O(g)和1.0mol CO(g),在一定条件下发生上述反应.混合气体中CO的物质的量与时间关系如下表所示:
相对实验Ⅰ,实验Ⅱ可能改变的条件可能是增大压强(或缩小体积)、加催化剂,该温度下,平衡常数=1.
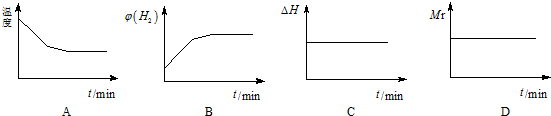
②若开始向绝热容器中投入一定量二氧化碳、氢气在一定条件下发生上述可逆反应.下列图象正确且说明可逆反应达到平衡状态的是A.(填序号)(Mr为反应混合物的平均相对分子质量)
(3)对燃煤烟气和汽车尾气进行脱硝、脱碳和脱硫等处理,可实现绿色环保、节能减排等目的.汽车尾气脱硝脱碳的主要原理为:2NO(g)+2CO(g)$\stackrel{催化剂}{?}$ N2(g)+2CO2(g)△H=-QkJ/mol.
一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
前2s内的平均反应速率υ(N2)=1.88×10-4mol/(L•s);
达到平衡时,CO的转化率为25%.
(4)氨气是重要化工原料,在国民经济中占重要地位.在恒温、容积相等的恒容密闭容器中投入一定量氮气、氢气,发生如下可逆反应:N2(g)+3H2(g)?2NH3(g)△H=-92.40kJ.mol-1 实验测得起始、平衡时的有关数据如表所示:
下列判断正确的是BC.
A.N2的转化率:Ⅱ>Ⅰ>ⅢB.放出热量:a<b<92.4n
C.达到平衡时氨气的体积分数:Ⅲ>ⅠD.平衡常数:Ⅲ>Ⅱ>Ⅰ
①2H2(g)+O2(g)=2H2O(l)△H1=-571.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ•mol-1
③CO(g)+2H2(g)?CH3OH(g)△H3=-90.8kJ•mol-1
计算甲醇蒸气的燃烧热△H=-763.8kJ•mol-1
(2)在某温度下,发生可逆反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.0kJ.mol-1
①向某容器中充入1.0molH2O(g)和1.0mol CO(g),在一定条件下发生上述反应.混合气体中CO的物质的量与时间关系如下表所示:
| 0 | 5min | 10min | 15min | 20min | 25min | |
| Ⅰ(800℃) | 1.0 | 0.80 | 0.70 | 0.65 | 0.50 | 0.50 |
| Ⅱ(800℃) | 1.0 | 0.7 | 0.60 | 0.50 | 0.50 | 0.50 |
②若开始向绝热容器中投入一定量二氧化碳、氢气在一定条件下发生上述可逆反应.下列图象正确且说明可逆反应达到平衡状态的是A.(填序号)(Mr为反应混合物的平均相对分子质量)

(3)对燃煤烟气和汽车尾气进行脱硝、脱碳和脱硫等处理,可实现绿色环保、节能减排等目的.汽车尾气脱硝脱碳的主要原理为:2NO(g)+2CO(g)$\stackrel{催化剂}{?}$ N2(g)+2CO2(g)△H=-QkJ/mol.
一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol•L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol•L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
达到平衡时,CO的转化率为25%.
(4)氨气是重要化工原料,在国民经济中占重要地位.在恒温、容积相等的恒容密闭容器中投入一定量氮气、氢气,发生如下可逆反应:N2(g)+3H2(g)?2NH3(g)△H=-92.40kJ.mol-1 实验测得起始、平衡时的有关数据如表所示:
| 容器编号 | 起始时各物质的物质的量/mol | 平衡时反应中的能量变化 | ||
| H2 | N2 | NH3 | ||
| Ⅰ | 3 n | n | 0 | 放出热量a kJ |
| Ⅱ | 3 n | 2 n | 0 | 放出热量b kJ |
| Ⅲ | 6 n | 2 n | 0 | 放出热量c kJ |
A.N2的转化率:Ⅱ>Ⅰ>ⅢB.放出热量:a<b<92.4n
C.达到平衡时氨气的体积分数:Ⅲ>ⅠD.平衡常数:Ⅲ>Ⅱ>Ⅰ
 如图所示的装置,接通电源5min后,电极3的质量增加了0.64g.
如图所示的装置,接通电源5min后,电极3的质量增加了0.64g.