题目内容
7.(1)已知:①2H2(g)+O2(g)=2H2O(l)△H1=-571.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ•mol-1
③CO(g)+2H2(g)?CH3OH(g)△H3=-90.8kJ•mol-1
计算甲醇蒸气的燃烧热△H=-763.8kJ•mol-1
(2)在某温度下,发生可逆反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.0kJ.mol-1
①向某容器中充入1.0molH2O(g)和1.0mol CO(g),在一定条件下发生上述反应.混合气体中CO的物质的量与时间关系如下表所示:
| 0 | 5min | 10min | 15min | 20min | 25min | |
| Ⅰ(800℃) | 1.0 | 0.80 | 0.70 | 0.65 | 0.50 | 0.50 |
| Ⅱ(800℃) | 1.0 | 0.7 | 0.60 | 0.50 | 0.50 | 0.50 |
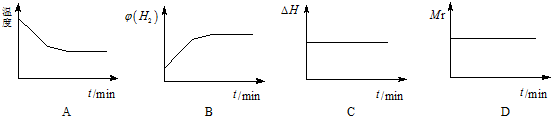
②若开始向绝热容器中投入一定量二氧化碳、氢气在一定条件下发生上述可逆反应.下列图象正确且说明可逆反应达到平衡状态的是A.(填序号)(Mr为反应混合物的平均相对分子质量)
(3)对燃煤烟气和汽车尾气进行脱硝、脱碳和脱硫等处理,可实现绿色环保、节能减排等目的.汽车尾气脱硝脱碳的主要原理为:2NO(g)+2CO(g)$\stackrel{催化剂}{?}$ N2(g)+2CO2(g)△H=-QkJ/mol.
一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol•L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol•L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
达到平衡时,CO的转化率为25%.
(4)氨气是重要化工原料,在国民经济中占重要地位.在恒温、容积相等的恒容密闭容器中投入一定量氮气、氢气,发生如下可逆反应:N2(g)+3H2(g)?2NH3(g)△H=-92.40kJ.mol-1 实验测得起始、平衡时的有关数据如表所示:
| 容器编号 | 起始时各物质的物质的量/mol | 平衡时反应中的能量变化 | ||
| H2 | N2 | NH3 | ||
| Ⅰ | 3 n | n | 0 | 放出热量a kJ |
| Ⅱ | 3 n | 2 n | 0 | 放出热量b kJ |
| Ⅲ | 6 n | 2 n | 0 | 放出热量c kJ |
A.N2的转化率:Ⅱ>Ⅰ>ⅢB.放出热量:a<b<92.4n
C.达到平衡时氨气的体积分数:Ⅲ>ⅠD.平衡常数:Ⅲ>Ⅱ>Ⅰ
分析 (1)①2H2(g)+O2(g)=2H2O(l)△H1=-571.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ•mol-1
③CO(g)+2H2(g)═CH3OH(g)△H3=-90.8kJ•mol-1
根据盖斯定律知,①+②×$\frac{1}{2}$-③得:CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l);
(2)①从数据看,I和II达到相同状态,说明平衡没有移动,若该可逆反应是等气体分子数反应,则增大压强,平衡不移动,或者加入催化剂也能加快反应速率,平衡不移动;
等气体分子数反应,可以用物质的量代替浓度计算平衡常数,达到平衡时,各物质的物质的量都等于0.5mol,根据K=$\frac{c(CO{\;}_{2})c(H{\;}_{2})}{c(CO)c(H{\;}_{2}O)}$计算;
②A、开始投入二氧化碳和氢气,从逆方向进行反应,反应吸热,开始温度下降,当温度不变时达到平衡状态;
B、开始投入二氧化碳和氢气,从逆方向进行反应,氢气体积分数由最大逐渐减小.
C、反应热只与化学计量数有关,与反应限度无关.
D、因为总质量不变,总物质的量也不变,根据混合气体平均相对分子质量=$\frac{m(总)}{n(总)}$判断;
(3)依据反应速率V=$\frac{△c}{△t}$计算一氧化碳的反应速率,结合反应速率之比等于化学方程式计量数之比计算氮气的反应速率,转化率=$\frac{消耗量}{起始量}$×100%;
(4)A、实验I和III比较,实验III相当于实验I体积压缩一半,加压时平衡向正方向移动,I、II实验中氢气量相等,氮气量越多,氮气转化率减小,据此回答;
B、根据可逆反应特点,3mol氢气和1mol氮气不能完全生成NH3;
C、根据压强对化学平衡移动的影响来回答;
D、温度不变,平衡常数不变.
解答 解:(1)①2H2(g)+O2(g)=2H2O(l)△H1=-571.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ•mol-1
③CO(g)+2H2(g)═CH3OH(g)△H3=-90.8kJ•mol-1
根据盖斯定律知,①+②×$\frac{1}{2}$-③得:CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)
△H=-571.6kJ•mol-1-566.0kJ•mol-1×$\frac{1}{2}$+90.8kJ•mol-1=-763.8kJ•mol-1,
故答案为:-763.8kJ•mol-1;
(2)①从数据看,I和II达到相同状态,说明平衡没有移动,若该可逆反应是等气体分子数反应,且反应物和产物都是气态,增大压强,平衡不移动,能缩短达到平衡的时间;加入催化剂也能加快反应速率,缩短达到平衡时间;
等气体分子数反应,可以用物质的量代替浓度计算平衡常数,达到平衡时,各物质的物质的量都等于0.5mol,所以K=$\frac{c(CO{\;}_{2})c(H{\;}_{2})}{c(CO)c(H{\;}_{2}O)}$=$\frac{0.5mol×0.5mol}{0.5mol×0.5mol}$=1,
故答案为:增大压强(或缩小体积)、加催化剂;1;
②A、开始投入二氧化碳和氢气,从逆方向进行反应,反应吸热,开始温度下降,当温度不变时达到平衡状态,故A正确;
B、开始投入二氧化碳和氢气,从逆方向进行反应,氢气体积分数由最大逐渐减小,故B错误.
C、反应热只与化学计量数有关,与反应限度无关,所以焓变一直不变,故C错误.
D、因为总质量不变,总物质的量也不变,所以混合气体平均相对分子质量=$\frac{m(总)}{n(总)}$始终不变,故D错误.
故选:A.
(3)前2s内的平均反应速率v(N2)=$\frac{1}{2}$v(CO)=$\frac{1}{2}$×$\frac{3.60×10{\;}^{-3}mol/L-2.85×10{\;}^{-3}mol/L}{2s}$=1.88×10-4mol/(L•s),
CO的平衡转化率=$\frac{3.60×10{\;}^{-3}mol/L-2.70××10{\;}^{-3}mol/L}{3.60×10{\;}^{-3}mol/L}$×100%=25%,
故答案为:1.88×10-4;25%;
(4)A、实验I和III比较,实验III相当于实验I体积压缩一半,加压时平衡向正方向移动,N2转化率增大,III中氮气转化率大于I中氮气转化率;I、II实验中氢气量相等,氮气量越多,氮气转化率减小,I中氮气转化率大于II中氮气转化率,故III、I、II中氮气转化率依次增大,A错误;
B、可逆反应的热化学方程式表示:1mol氮气和3mol氢气完全反应放出92.4kJ热量.根据可逆反应特点,3mol氢气和1mol氮气不能完全生成NH3.II生成的氨气量大于I,B项正确;
C、如果平衡不移动,III中氨气量是I中2倍,氨气体积分数相等.在恒容条件下,I容器加压变成III,增大压强,平衡向生成NH3方向移动,氨体积分数增大,C正确;
D、温度不变,平衡常数不变,三个容器中平衡常数相等,D错误.
故选BC.
点评 本题考查化学平衡的标志、平衡常数的计算及化学平衡移动原理、盖斯定律的计算应用等,知识点较多,综合性很强,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | NaCl | B. | AlCl3 | C. | CaCl2 | D. | FeCl3 |
| t/s | 0 | 500 | 1 000 |
| c(H2)/mol•L-1 | 5.00 | 3.52 | 2.48 |
| c(CO)/mol•L-1 | 2.50 |
(2)在1 000s内用CO表示的化学反应速率是1.26×10-3mol/(L•s),1 000s时CO的转化率是50.4%.
(3)在500s时生成的甲醇的浓度是0.74mol/L.
(4)下列叙述能说明该反应已达到化学平衡状态的是(填标号)ADE;
A.容器内的总压强不随时间而变化
B.反应后混合气体的密度不再发生变化
C.三种气体的浓度相等
D.CH3OH的分解速率与生成速率相等
E.混合气体的平均相对分子质量不再发生变化.
| T/℃ | 30 | 40 | 50 | 60 |
| NH3生成量/10-6 mol | 4.8 | 5.9 | 6.0 | 6.1 |

回答下列问题:
(1)请画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化的示意图,并进行必要标注.
(2)与目前广泛使用的工业合成氨方法相比,该方法固氮反应速率慢.请提出可提高其反应速率且增大NH3生成量的建议:升高温度,增大反应物N2的浓度,不断移出生成物脱离反应体系.
(3)工业合成氨的反应为N2(g)+3H2(g)高温、高压催化剂
2NH3(g).设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数为$\frac{4}{7}$.
①该条件下N2的平衡转化率为66.7%
②该条件下反应2NH3(g)高温、高压催化剂N2(g)+3H2(g)的平衡常数为0.005.
| 操作和现象 | 结论 | |
| A | 取某溶液少许,加入酸化的Ba(NO3)2溶液,产生白色沉淀 | 该溶液一定含SO42- |
| B | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 结合H+的能力:CO32-<AlO2- |
| C | 某溶液加入盐酸产生使石灰水变浑浊的无色无味气体 | 该溶液肯定含HCO3-、CO32-中的一种或二种 |
| D | 测定等浓度的Na2CO3和Na2SO3溶液的pH;前者pH比后者的大; | 非金属性:S>C |
| A. | A | B. | B | C. | C | D. | D |
| A. | 0.05NA | B. | 0.1NA | ||
| C. | 0.15NA | D. | 条件不足,不能计算 |

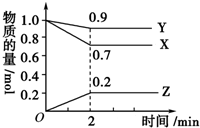 某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示.由图中数据分析,该反应的化学方程式为Y+3X?2Z,反应开始至2min,X的转化率为30%.
某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示.由图中数据分析,该反应的化学方程式为Y+3X?2Z,反应开始至2min,X的转化率为30%.