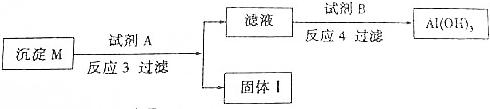
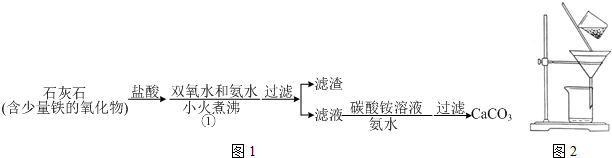
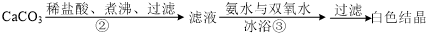题目内容
11.在一个容积不变的密闭容器中,发生反应:2NO(g)+O2(g)?2NO2(g)(1)当n(NO):n(O2)=4:1时,O2的转化率随时间的变化关系如图1所示.
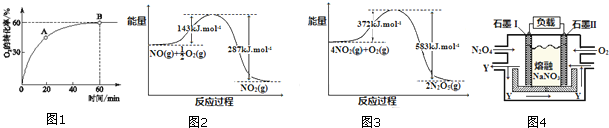
①A点的逆反应速率v逆 (O2)小于B点的正反应速率v正(O2)(填“大于”、“小于”或“等于”).
②NO的平衡转化率为30%;当达到B点后往容器中再以4:1加入些NO和 O2,当达到新平衡时,则NO的百分含量小于B点NO的百分含量(填“大于”、“小于”或“等于”).
③到达B点后,下列关系正确的是ABCD. A.容器内气体颜色不再变化 B.v正(NO)=2v正(O2)
C.气体平均摩尔质量在此条件下达到最大 D.容器内气体密度不再变化
(2)在图2和图3中出现的所有物质都为气体,分析图2和图3,可推测:
4NO(g)+3O2(g)=2N2O5(g)△H=-787kJ/mol
(3)降低温度,NO2(g)将转化为N2O4(g),以N2O4、O2、熔融NaNO3组成的燃料电池装置如图4所示,在使用过程中石墨I电极反应生成一种氧化物Y,Y为N2O5,有关石墨I电极反应式可表示为:N2O4+2NO3--2e-=2N2O5.
分析 (1)①A到B点氧气的转化率增大,说明反应正向进行;
②平衡时压强转化率为60%,当n(NO):n(O2)=4:1时设NO为4,O2为1,结合化学平衡三行计算得到;当达到B点后往容器中再以4:1加入些NO和 O2,相当于中等容器中气体压强,平衡正向进行;
③到达B点即达到平衡状态,正逆反应速率相同,各组分含量保持不变;
(2)依据图象分别写出对应反应的热化学方程式,结合盖斯定律计算4NO(g)+3O2(g)═2N2O5(g)反应的焓变;
(3)燃料原电池中,负极上燃料失电子发生氧化反应;先根据化合价判断生成氧化物N2O5的电极,再根据离子的放电顺序写出电极反应式.
解答 解:(1)①A到B点氧气的转化率增大,说明反应正向进行,A点的逆反应速率v逆 (O2)小于B点的正反应速率v正(O2),
故答案为:小于;
②平衡时压强转化率为60%,当n(NO):n(O2)=4:1时设NO为4,O2为1,则转化的氧气为0.6,结合化学平衡三行计算,
2NO(g)+O2(g)═2NO2(g)
起始量 4 1 0
变化量 1.2 0.6 1.2
平衡量 2.8 0.4 1.2
NO的平衡转化率$\frac{1.2}{4}$×100%=30%,
当达到B点后往容器中再以4:1加入些NO和 O2,相当于中等容器中气体压强,平衡正向进行,一氧化氮百分含量减小,NO的百分含量小于B点NO的百分含量,
故答案为:30%;小于;
③2NO(g)+O2(g)═2NO2(g)反应是气体体积进行的放热反应,
A.容器内气体颜色不再变化,说明二氧化氮浓度不变,反应达到平衡状态,故A正确;
B.速率之比等于化学方程式计量数之比为正反应速率之比,反应达到平衡状态v正(NO)=2v正(O2),故B正确;
C.达到平衡状态气体质量不变,物质的量不变,气体平均摩尔质量在此条件下达到最大,故C正确;
D.达到平衡状态,容器内气体密度不再变化,故D正确;
故答案为:ABCD;
(2)热化学方程式为①NO(g)+$\frac{1}{2}$O2(g)=NO2(g)△H=143KJ/mol-287KJ/mol=-144KJ/mol,
②4NO2(g)+O2(g)=2N2O5(g)△H=(372-583)KJ/mol=-211KJ/mol,
依据盖斯定律计算①×4+②得到4NO(g)+3O2(g)═2N2O5(g)△H=-787kJ/mol,
故答案为:-787kJ/mol;
(3)以N2O4、O2、熔融NaNO3组成的燃料电池装置如下图所示,在使用过程中石墨I电极反应生成一种氧化物Y,N2O4在负极失电子发生氧化反应,元素化合价升高为+5价,氧化物为N2O5,反应的电极反应为:N2O4+2NO3--2e-=2 N2O5,
故答案为:N2O5;N2O4+2NO3--2e-=2 N2O5.
点评 本题综合考查图象分析、化学平衡影响因素、平衡标志的判断、平衡计算、热化学方程式书写、原电池原理等知识点,为高考常见题型和高频考点,侧重于学生的分析能力和计算能力的考查,本题注意把握化学平衡的计算方法,答题时把握做题思路,难度中等.

(1)写出浓硫酸与木炭反应方程式,并标明电子转移的方向和数目:
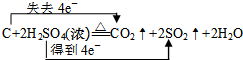 .
.【装置设计】组装如下的实验装置,然后进行实验探究.
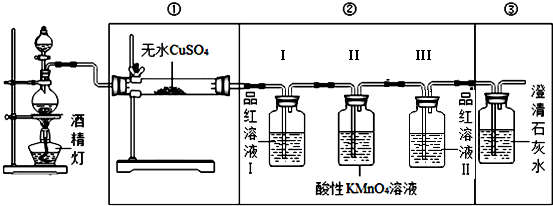
(2)装入反应物之前,必须先检验装置气密性.
【实验探究】
(3)观察实验,完成实验现象的部分记录:
| 实验装置 | ① | ③ |
| 实验现象 |
(1)上述反应的化学平衡常数表达式为$\frac{{c}^{3}({H}_{2}O)}{{c}^{3}({H}_{2})}$.
(2)某温度下反应达到平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为60%;随着温度的升高,H2与水蒸气的体积比减小,则该反应为吸热反应(填“吸热”或“放热”).
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成分 | WO3 W2O5 WO2 W |
(4)已知:温度过高时,WO2(s)转变为WO2(g):
WO2(s)+2H2(g)?W(s)+2H2O (g)△H=+66.0kJ?mol-1
WO2(g)+2H2(g)?W(s)+2H2O (g)△H=-137.9kJ?mol-1
则WO2(s)?WO2(g)的△H=+203.9 kJ•mol-1.
(5)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W(s)+2I2 (g) $?_{约3000℃}^{1400℃}$WI4 (g).下列说法正确的有a、b.
a.灯管内的I2可循环使用
b.WI4在灯丝上分解,产生的W又沉积在灯丝上
c.WI4在灯管壁上分解,使灯管的寿命延长
d.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢.
 l·L-1
l·L-1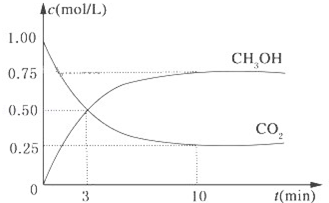 降低大气中CO2的含量及有效地开发利用 CO2,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示.
降低大气中CO2的含量及有效地开发利用 CO2,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示.