题目内容
兴趣小组的学生根据Mg与CO2反应原理推测Na也能在CO2中燃烧,为了确定其产物并进行实验论证,某同学设计了图甲装置进行实验(已知PdCl2能被CO还原得到黑色的Pd).请回答下列问题:
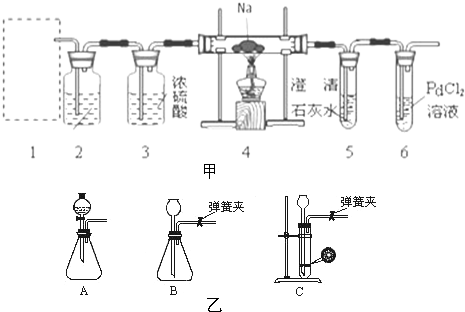
(1)图甲装置2中应盛放 溶液.
(2)为了使反应随开随用,随关随停,如图方框内应选用 装置(填图乙中字母代号).
(3)检查装置的气密性完好并装好药品后,在点燃酒精灯前,应先进行装置1中的反应操作,待装置 (填数字编号)中出现 现象时,再点酒精灯,这步操作的目的是 .
(4)①若装置6中有黑色沉淀生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为 .
②若装置6中溶液无明显现象,装置4中残留固体(有两种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为 .
(5)指导老师认为,不仅要检验残留固体中是否有碳酸钠还要检验其中是否有氧化钠和碳.当确认钠充分反应后,请你设计一个简单实验,验证装置4中的残留固体中是否有Na2O和C: .

(1)图甲装置2中应盛放
(2)为了使反应随开随用,随关随停,如图方框内应选用
(3)检查装置的气密性完好并装好药品后,在点燃酒精灯前,应先进行装置1中的反应操作,待装置
(4)①若装置6中有黑色沉淀生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为
②若装置6中溶液无明显现象,装置4中残留固体(有两种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为
(5)指导老师认为,不仅要检验残留固体中是否有碳酸钠还要检验其中是否有氧化钠和碳.当确认钠充分反应后,请你设计一个简单实验,验证装置4中的残留固体中是否有Na2O和C:
考点:碱金属及其化合物的性质实验
专题:几种重要的金属及其化合物
分析:(1)由实验方案图可知装置2是除去二氧化碳中的HCl,应用饱和的碳酸氢钠溶液;
(2)制取二氧化碳时,为了使制气过程具有“随开随用,随关随停”的特点,应该选用能够可以固、液药品分开的装置;
(3)由实验方案图可知,1为二氧化碳发生装置,4为二氧化碳与钠反应装置,加入4装置的二氧化碳应干燥,没有其它,故装置2是除去二氧化碳其它中的HCl,应用饱和的碳酸氢钠溶液,3为干燥装置,吸收水蒸气.反应需要排尽装置内的空气,当5装置中产生白色沉淀,说明空气中的二氧化碳排尽,再加热4处的酒精灯发生反应;
(4)①由题意可知,装置4中的残留固体(只有一种物质)加盐酸有能使石灰水变浑浊的气体放出,说明生成碳酸钠,装置6中有黑色沉淀,说明PdCl2溶液能被CO还原得到黑色的Pd,所以反应物为碳酸钠和CO;
②装置4中残留固体(有两种物质)加盐酸有能使石灰水变浑浊的气体放出,其中一种固体为碳酸钠,另一种固体为C;
(5)根据C不溶于水分析.
(2)制取二氧化碳时,为了使制气过程具有“随开随用,随关随停”的特点,应该选用能够可以固、液药品分开的装置;
(3)由实验方案图可知,1为二氧化碳发生装置,4为二氧化碳与钠反应装置,加入4装置的二氧化碳应干燥,没有其它,故装置2是除去二氧化碳其它中的HCl,应用饱和的碳酸氢钠溶液,3为干燥装置,吸收水蒸气.反应需要排尽装置内的空气,当5装置中产生白色沉淀,说明空气中的二氧化碳排尽,再加热4处的酒精灯发生反应;
(4)①由题意可知,装置4中的残留固体(只有一种物质)加盐酸有能使石灰水变浑浊的气体放出,说明生成碳酸钠,装置6中有黑色沉淀,说明PdCl2溶液能被CO还原得到黑色的Pd,所以反应物为碳酸钠和CO;
②装置4中残留固体(有两种物质)加盐酸有能使石灰水变浑浊的气体放出,其中一种固体为碳酸钠,另一种固体为C;
(5)根据C不溶于水分析.
解答:
解:(1)由实验方案图可知,1为二氧化碳发生装置,4为二氧化碳与钠反应装置,加入4装置的二氧化碳应干燥,没有其它,故装置2是除去二氧化碳中的HCl,应用饱和的碳酸氢钠溶液,
故答案为:饱和碳酸氢钠;
(2)制取二氧化碳时,为了使制气过程具有“随开随用,随关随停”的特点,应该选用能够可以固、液药品分开的装置,A中只能控制反应的速率,但不能控制反应的随时进行与停止;而C中当打开止水夹时,酸就和有孔塑料板上的石灰石反应生成气体,当关闭止水夹时,生成的气体就无法从导管中排出,从而使装置内的压强增大,把酸液挤到长颈漏斗中,使固液分离,故选C;
(3)由分析可知,反应需要排尽装置内的空气,当装置5中澄清的石灰水变浑浊,说明空气中的二氧化碳排尽,再加热4处的酒精灯发生反应,
故答案为:5;澄清的石灰水变浑浊;驱除系统内的空气;
(4)①由题意可知,装置4中的残留固体(只有一种物质)加盐酸有能使石灰水变浑浊的气体放出,说明生成碳酸钠,装置6中有黑色沉淀,说明PdCl2溶液能被CO还原得到黑色的Pd,所以反应物为碳酸钠和CO,反应的化学方程式为2Na+2CO2=Na2CO3+CO,故答案为:2Na+2CO2=Na2CO3+CO;
②装置4中残留固体(有两种物质)加盐酸有能使石灰水变浑浊的气体放出,其中一种固体为碳酸钠,另一种固体为C,反应的方程式为4Na+3CO2=2Na2CO3+C,
故答案为:4Na+3CO2=2Na2CO3+C;
(5)根据C不溶于水分析,将4中固体加足量水,有不溶黑色固体,则生成物中有C,
故答案为:将4中固体加足量水,有不溶黑色固体,则生成物中有C,在所得水溶液中加入过量BaCl2溶液,有沉淀生成,说明有Na2CO3生成;过滤,用pH试纸检验滤液,若滤液呈碱性,则残留固体中含有Na2O.
故答案为:饱和碳酸氢钠;
(2)制取二氧化碳时,为了使制气过程具有“随开随用,随关随停”的特点,应该选用能够可以固、液药品分开的装置,A中只能控制反应的速率,但不能控制反应的随时进行与停止;而C中当打开止水夹时,酸就和有孔塑料板上的石灰石反应生成气体,当关闭止水夹时,生成的气体就无法从导管中排出,从而使装置内的压强增大,把酸液挤到长颈漏斗中,使固液分离,故选C;
(3)由分析可知,反应需要排尽装置内的空气,当装置5中澄清的石灰水变浑浊,说明空气中的二氧化碳排尽,再加热4处的酒精灯发生反应,
故答案为:5;澄清的石灰水变浑浊;驱除系统内的空气;
(4)①由题意可知,装置4中的残留固体(只有一种物质)加盐酸有能使石灰水变浑浊的气体放出,说明生成碳酸钠,装置6中有黑色沉淀,说明PdCl2溶液能被CO还原得到黑色的Pd,所以反应物为碳酸钠和CO,反应的化学方程式为2Na+2CO2=Na2CO3+CO,故答案为:2Na+2CO2=Na2CO3+CO;
②装置4中残留固体(有两种物质)加盐酸有能使石灰水变浑浊的气体放出,其中一种固体为碳酸钠,另一种固体为C,反应的方程式为4Na+3CO2=2Na2CO3+C,
故答案为:4Na+3CO2=2Na2CO3+C;
(5)根据C不溶于水分析,将4中固体加足量水,有不溶黑色固体,则生成物中有C,
故答案为:将4中固体加足量水,有不溶黑色固体,则生成物中有C,在所得水溶液中加入过量BaCl2溶液,有沉淀生成,说明有Na2CO3生成;过滤,用pH试纸检验滤液,若滤液呈碱性,则残留固体中含有Na2O.
点评:本题联系学生感兴趣的实际新知识,有助于学生能力的考查,必须活学活用才能解好这类有新意的试题.

练习册系列答案
相关题目
V L浓度为0.5mol?L-1的盐酸,欲使其浓度增大1倍,采取的措施合理的是( )
| A、通入标准状况下的HCl气体11.2V L |
| B、加入10 mol?L-1的盐酸0.1V L,再稀释至1.5V L |
| C、将溶液加热浓缩到0.5V L |
| D、加入V L 1.5 mol?L-1的盐酸混合均匀 |
把下列四种X溶液分别加入四个盛有10mL 2mol/L盐酸的烧杯中,X和盐酸缓慢地进行反应,其中反应最快的是( )
| A、10℃200mL 3mol/L的X溶液 |
| B、20℃300mL 2mol/L的X溶液 |
| C、20℃10mL 4mol/L的X溶液 |
| D、10℃10mL 2mol/L的X溶液 |
碱金属的氧化物在氯气作用下很容易转变成氯化物,如在密闭容器中发生反应:2K2O+2Cl2?4KCl+O2,下列说法不正确的是( )
| A、上述反应属于置换反应 |
| B、升高温度,v(正)、v(逆)均增大 |
| C、缩小容器体积,v(正)、v(逆)均增大 |
| D、反应足够长时间后,密闭容器只含O2一种气体 |

 已知:一个碳原子上连两个羟基时自动脱水形成醛基,即:
已知:一个碳原子上连两个羟基时自动脱水形成醛基,即: 现有A~F六种有机物,存在如图所示的转化关系.据此完成下列问题:
现有A~F六种有机物,存在如图所示的转化关系.据此完成下列问题: