题目内容
8.在N2+3H2?2NH3的反应中,经过一段时间后,NH3的浓度增加0.6mol/L,在此时间内用H2表示的平均反应速率为0.45mol/(L•s),则所经历的时间是( )| A. | 0.27 s | B. | 0.44 s | C. | 1.33 s | D. | 2 s |
分析 在N2+3H2?2NH3的反应中,经过一段时间后,NH3的浓度增加0.6mol/L,根据方程式知,氢气浓度减少$\frac{3}{2}$×0.6mol/L=0.9mol/L,在此时间内用H2表示的平均反应速率为0.45mol/(L•s),则所经历的时间=$\frac{△c}{v}$,据此分析解答.
解答 解:在N2+3H2?2NH3的反应中,经过一段时间后,NH3的浓度增加0.6mol/L,根据方程式知,氢气浓度减少$\frac{3}{2}$×0.6mol/L=0.9mol/L,在此时间内用H2表示的平均反应速率为0.45mol/(L•s),则所经历的时间=$\frac{△c}{v}$=$\frac{0.9mol/L}{0.45mol/(L.s)}$=2s,故选D.
点评 本题考查化学反应速率有关计算,侧重考查学生分析计算能力,明确同一时间段内各物质浓度变化量与计量数关系是解本题关键,题目难度不大.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
19.1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
| A. | 得到2.54 g沉淀时,加入NaOH溶液的体积是700 mL | |
| B. | 该合金中铜与镁的物质的量之比是2:1 | |
| C. | 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L | |
| D. | NO2和N2O4的混合气体中,NO2的体积分数是80% |
3.现有部分短周期元素的性质或原子结构如下表:
(1)用化学用语回答下列问题:
①A元素在周期表中的位置第三周期第ⅥA族;
②用电子式表示A和B元素组成的化合物的形成过程 .
.
(2)元素D与元素A相比,D非金属性较强,下列表述中能证明这一事实的是bde.
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一.A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是NaOH(写化学式).
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为W(其他条件略去).
X$\stackrel{O_{2}}{→}$Y$\stackrel{O_{2}}{→}$Z$\stackrel{H_{2}O}{→}$W
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为:BaSO4;生成该白色沉淀的化学方程式为BaCl2+SO2+H2O2=BaSO4↓+2HCl.
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为1:2.
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素高正价是+7价 |
①A元素在周期表中的位置第三周期第ⅥA族;
②用电子式表示A和B元素组成的化合物的形成过程
 .
.(2)元素D与元素A相比,D非金属性较强,下列表述中能证明这一事实的是bde.
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一.A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是NaOH(写化学式).
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为W(其他条件略去).
X$\stackrel{O_{2}}{→}$Y$\stackrel{O_{2}}{→}$Z$\stackrel{H_{2}O}{→}$W
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为:BaSO4;生成该白色沉淀的化学方程式为BaCl2+SO2+H2O2=BaSO4↓+2HCl.
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为1:2.
20.下列实验操作正确的是( )
| A. | Na2S2O3与硫酸反应的实验中,实验室没有硫酸,临时用硝酸进行实验 | |
| B. | 滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定 | |
| C. | 制取氯气时,用二氧化锰与浓盐酸在加热下反应,并用排水集气法收集 | |
| D. | 配制FeCl3溶液时,将FeCl3溶解在较浓的盐酸中,用水稀释到所需浓度 |
17.下列有关化学用语表示正确的是( )
| A. | 四氯化碳分子的比例模型 | B. | 次氯酸的结构式为H-Cl-O | ||
| C. | CO2的电子式是: | D. | ${\;}_{8}^{18}$O2-离子结构示意图: |
 天然气(主要成分甲烷)含有少量含硫化合物[硫化氢、羰基硫(COS)、乙硫醇(C2H5SH)],可以用氢氧化钠溶液洗涤除去.
天然气(主要成分甲烷)含有少量含硫化合物[硫化氢、羰基硫(COS)、乙硫醇(C2H5SH)],可以用氢氧化钠溶液洗涤除去.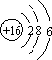 ;羰基硫分子的电子式为
;羰基硫分子的电子式为 .
.
