题目内容
17.X、Y、Z、M、N是原子序数依次增大的短周期主族元素,其中X与Z为同族元素,Y和M为同族元素,且Y与M的核外电子数之和为X和Z元素的核外电子数之和的2倍,下列说法正确的是( )| A. | 原子半径:Z>M>N>X>Y | B. | M与N形成的化合物中N显正价 | ||
| C. | 单质沸点:Z>M>N>Y>X | D. | 最高正价:N>M=Y>Z=X |
分析 X、Y、Z、M、N是原子序数依次增大的短周期主族元素,其中X与Z为同族元素,Y和M为同族元素,因为Y与M的核外电子数之和为X和Z元素的核外电子数之和的2倍,则X和Y不能都是第二周期元素,则X为H元素,Z为Na元素,H和Na元素核外电子数之和为12,它的二倍是24,Y和M同一主族且二者原子序数之和为24,则Y为O元素、M为S元素,N为短周期主族元素且原子序数大于S,所以N为Cl元素,
则X、Y、Z、M、N分别是H、O、Na、S、Cl元素;
A.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小;
B.M、N形成的化合物中,非金属性强的元素显负化合价;
C.单质熔沸点:金属晶体>分子晶体,分子晶体:固态>气态,气体单质熔沸点与其相对分子质量成正比;
D.主族元素最高正化合价与其族序数相等,但O、F元素除外.
解答 解:X、Y、Z、M、N是原子序数依次增大的短周期主族元素,其中X与Z为同族元素,Y和M为同族元素,因为Y与M的核外电子数之和为X和Z元素的核外电子数之和的2倍,则X和Y不能都是第二周期元素,则X为H元素,Z为Na元素,H和Na元素核外电子数之和为12,它的二倍是24,Y和M同一主族且二者原子序数之和为24,则Y为O元素、M为S元素,N为短周期主族元素且原子序数大于S,所以N为Cl元素,
则X、Y、Z、M、N分别是H、O、Na、S、Cl元素;
A.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径Z>M>N>Y>X,故A错误;
B.M、N形成的化合物中,非金属性强的元素显负化合价,非金属性N>M,所以M与N形成的化合物中N显负价,故B错误;
C.单质熔沸点:金属晶体>分子晶体,分子晶体:固态>气态,气体单质熔沸点与其相对分子质量成正比,所以这几种元素单质沸点:Z>M>N>Y>X,故C正确;
D.主族元素最高正化合价与其族序数相等,但O、F元素除外,O元素没有正化合价,故D错误;
故选C.
点评 本题考查原子结构和元素周期律,为高频考点,侧重考查学生分析判断及元素周期律的灵活运用,正确推断元素是解本题关键,知道单质熔沸点影响因素、化合价与族序数的关系,易错选项是D.

| A. | c(B2-)+c(HB-)=0.1 mol/L | B. | c(B2-)+c(HB-)+c(H2B)=0.1 mol/L | ||
| C. | c(OH-)=c(H+)+c(HB-)+2c(H2B) | D. | c(Na+)+c(OH-)=c(H+)+c(HB-) |
①BF3 ②CH3═CH2 ③苯 ④CH≡CH ⑤NH3 ⑥CH4 ⑦HCHO.
| A. | ①②③⑦ | B. | ①⑤⑥ | C. | ②③④⑦ | D. | ③⑤⑥ |
| A. | 电解质不一定能导电 | |
| B. | 氨溶于水得到的氨水能导电,所以氨水是电解质 | |
| C. | 将硫酸钡放入水中不能导电,所以硫酸钡是非电解质 | |
| D. | 在水溶液或熔融状态下能导电的物质叫做电解质 |
| A. | 氯水的颜色呈浅绿色,说明氯水中含有Cl2 | |
| B. | 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- | |
| C. | 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有 H+ | |
| D. | 新制的氯水能使红色布条褪色,说明氯水中含有Cl2 |
| A. | 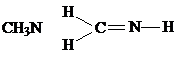 | B. | 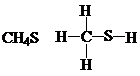 | ||
| C. |  | D. | 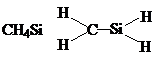 |
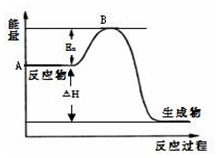 2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答:
2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答:
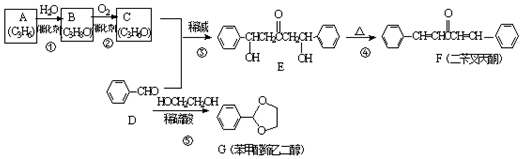
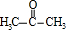 ;A加聚产物的结构简式是
;A加聚产物的结构简式是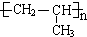 .
.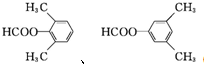 .
.