题目内容
 如图为用惰性电极电解CuCl2溶液,并验证其产物的实验装置,则下列说法不正确的是( )
如图为用惰性电极电解CuCl2溶液,并验证其产物的实验装置,则下列说法不正确的是( )| A、电源a极为负极 |
| B、KI-淀粉溶液会变蓝 |
| C、可以将惰性电极Ⅰ换为铜棒 |
| D、惰性电极Ⅰ上发生的电极反应为:Cu-2e-=Cu2+ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:用惰性电极电解CuCl2溶液,并验证其产物的实验装置,则II电极生成氯气为阳极,对应的b为正极;则a为负极,I为阴极,电解CuCl2溶液,在阴极铜离子放电生成Cu,阳极氯离子放电生成Cl2,以此解答该题.
解答:
解:用惰性电极电解CuCl2溶液,并验证其产物的实验装置,则II电极生成氯气为阳极,对应的b为正极;则a为负极,I为阴极,电解CuCl2溶液,在阴极铜离子放电生成Cu,阳极氯离子放电生成Cl2,
A.根据以上分析可知a为负极,b为正极,故A正确;
B.氯气与碘化钾反应生成单质碘,所以KI-淀粉溶液会变蓝,故B正确;
C.根据以上分析可知,I为阴极,阴极上电极本身不参加反应,所以能用活性电极作阴极,故可以将惰性电极Ⅰ换为铜棒,故C正确;
D.I为阴极,阴极上阳离子得电子,所以惰性电极Ⅰ上发生的电极反应为:Cu2++2e-=Cu,故D错误,
故选D.
A.根据以上分析可知a为负极,b为正极,故A正确;
B.氯气与碘化钾反应生成单质碘,所以KI-淀粉溶液会变蓝,故B正确;
C.根据以上分析可知,I为阴极,阴极上电极本身不参加反应,所以能用活性电极作阴极,故可以将惰性电极Ⅰ换为铜棒,故C正确;
D.I为阴极,阴极上阳离子得电子,所以惰性电极Ⅰ上发生的电极反应为:Cu2++2e-=Cu,故D错误,
故选D.
点评:本题考查电解原理,题目难度不大,本题注意把握电解池的两极的判断,为解答该题的关键,注意电解时两极的变化.

练习册系列答案
相关题目
NA表示阿伏加德罗常数,下列判断正确的是( )
| A、含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol?L-1 |
| B、1L0.1mol?L-1的氨水含有0.1NA个NH3?H2O |
| C、5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等 |
| D、10LpH=1的硫酸溶液中含有的H+离子数为2NA |
下列说法不正确的是( )
| A、铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
| C、一定条件下,使用催化剂能加快反应速率 |
| D、相同条件下,溶液中Fe3+、Cu2+、Zn2+的氧化性依次减弱 |
某化合物6.4g在氧气中完全燃烧,只生成8.8g CO2和7.2g H2O.下列说法正确的是( )
| A、该化合物仅含碳、氢两种元素 |
| B、该化合物中碳、氢原子个数比为1:4 |
| C、无法确定该化合物是否含有氧元素 |
| D、该化合物一定是C2H8O2 |
下列反应的离子方程式不正确的是( )
| A、用盐酸清除水垢CaCO3+2H+=Ca2++CO2↑+H2O |
| B、Fe跟稀硫酸反应:Fe+2H+=Fe2++H2↑ |
| C、Na2O2投入水中 2Na2O2+2H2O=4Na++4OH-+O2↑ |
| D、碳酸氢钠溶液跟氢氧化钠溶液反应 HCO3-+OH-=H2O+CO2↑ |
 已知[Co(NH3)6]3+呈正八面体结构,若其中有两个NH3分子分别被H2O取代,所形成的[Co(NH3)4(H2O)2]3+的几何异构体种数有几种(不考虑光学异构)( )
已知[Co(NH3)6]3+呈正八面体结构,若其中有两个NH3分子分别被H2O取代,所形成的[Co(NH3)4(H2O)2]3+的几何异构体种数有几种(不考虑光学异构)( )| A、2种 | B、3种 | C、4种 | D、6种 |
下列事实,不能用勒夏特列原理解释的是( )
| A、氯水中有下列平衡:Cl2+H2O?HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅 |
| B、对于2HI(g)?H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色加深 |
| C、合成氨工业中,为提高氨的产率,采用10~30MPa的压强 |
| D、反应CO(g)+NO2(g)?CO2(g)+NO(g)△H<0,达平衡后,升高温度体系颜色变深 |
有机物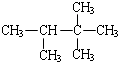 的名称是( )
的名称是( )
 的名称是( )
的名称是( )| A、2,3,3-三甲基丁烷 |
| B、2,3-三甲基丁烷 |
| C、2,2,3-三甲基丁烷 |
| D、2,3-三甲基丁烷 |
 如图为PCl5(g)?PCl3(g)+Cl2(g)(正反应为吸热反应),从平衡状态Ⅰ移动到平衡状态Ⅱ的反应速率(v)与时间(t)的曲线,此图表示的变化是( )
如图为PCl5(g)?PCl3(g)+Cl2(g)(正反应为吸热反应),从平衡状态Ⅰ移动到平衡状态Ⅱ的反应速率(v)与时间(t)的曲线,此图表示的变化是( )| A、降温 |
| B、降压 |
| C、增加PCl5的量 |
| D、增加PCl3的量 |