题目内容
如图所示各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由快到慢的顺序为( )

| A、⑤②①④③ |
| B、③②⑤④① |
| C、⑤④②③① |
| D、⑤②①③④ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:先判断装置是原电池还是电解池,再根据原电池正负极腐蚀的快慢比较,从而确定腐蚀快慢顺序,电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀.
解答:
解:根据图知,②③装置是原电池,在②中,金属铁做负极,③中金属铁作正极,做负极的腐蚀速率快,所以②>③,并且原电池原理引起的腐蚀>化学腐蚀,所以②>①,④⑤装置是电解池,⑤中金属铁为阳极,④中金属铁为阴极,阳极金属被腐蚀速率快,阴极被保护,即⑤>④,根据电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀,并且原电池的正极金属腐蚀速率快于电解池的阴极金属腐蚀速率,即⑤②①③④,故答案为:D.
点评:不同条件下金属腐蚀的快慢:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀.

练习册系列答案
相关题目
下列物质久置于空气中,颜色发生变化的( )
| A、Na2SO4 |
| B、苯酚 |
| C、Na2O2 |
| D、CaO |
在某温度下,将某NaOH溶液和0.1mol/L的CH3COOH溶液充分混合后,若溶液呈中性,则该混合溶液中有关离子的浓度应满足的关系是( )
| A、c(H+)=c(OH-)=1×10-7mol/L |
| B、c(Na+)>c(CH3COO-) |
| C、c(Na+)<c(CH3COO-) |
| D、c(Na+)-c(CH3COO-)=0 |
在0.1mol/L NaHCO3溶液中,下列关系式错误的是( )
| A、c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
| B、c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-) |
| C、c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
| D、c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) |
最新研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )
| A、羰基硫属于非极性分子 |
| B、羰基硫的结构式为:S=C=O |
| C、羰基硫与CO2不是等电子体 |
| D、羰基硫分子中三个原子不处于同一直线上 |
 夜幕降临,北京奥运会主会场“鸟巢”内灯火辉煌,鼓瑟齐鸣.璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应.鸟巢夜景照明由五个部分组成,其中主体照明以传统文化元素“中国红”为主色.请回答下列问题:
夜幕降临,北京奥运会主会场“鸟巢”内灯火辉煌,鼓瑟齐鸣.璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应.鸟巢夜景照明由五个部分组成,其中主体照明以传统文化元素“中国红”为主色.请回答下列问题: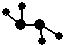 ,C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题:
,C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题: