题目内容
某溶液中含有大量的下列离子:Fe3+、SO42-、A13+和M离子,经测定Fe3+、SO42-、A13+和M离子的物质的量之比为2:3:1:3,则M离子可能是下列中的( )
| A、Na+ |
| B、OH- |
| C、S2- |
| D、C1- |
考点:离子共存问题
专题:离子反应专题
分析:溶液中一定满足电荷守恒,根据电荷守恒判断M离子所带电荷,然后根据离子能否大量共存判断可能存在的离子.
解答:
解:根据题目条件和电荷守恒可知:3n(Fe3+)×2+3n(Al3+)×1=2n(SO42-)×2+3n(M),即:2×3+3×1=2×3+3M,M=1,M带有1个单位的负电荷,
又OH-离子不能与铁离子大量共存,所以M只能为选项中的Cl-离子.
故选D.
又OH-离子不能与铁离子大量共存,所以M只能为选项中的Cl-离子.
故选D.
点评:本题考查离子共存的正误判断,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况,本题侧重考查电荷守恒的应用.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
下列有关电解的说法正确的是( )
| A、用惰性电极电解饱和食盐水初期,只需在溶液中加入适量的盐酸即可恢复至原溶液 | ||||
| B、工业上用电解熔融的氯化镁冶炼镁,也可采用电解熔融的氯化铝冶炼铝 | ||||
| C、工业用电解法进行粗铜精炼时,每转移1mol电子,阳极上就溶解0.5NA个铜原子 | ||||
D、用惰性电极电解CuSO4溶液,有可能发生Cu2++2H2O
|
下列化合物中,氯元素的化合价为+5价的是( )
| A、HCl |
| B、NaCl |
| C、KClO3 |
| D、KClO4 |
下列各组离子一定能大量共存的是( )
| A、在含有大量[Al(OH)4]-的溶液中:NH4+、Na+、Cl-、H+ |
| B、在c(H+)=0.1mol?L-1的溶液中:K+、I-、Cl-、NO3- |
| C、在pH=12的溶液中:NH4+、Na+、SO42-、Cl- |
| D、在强碱溶液中:Na+、K+、CO32-、NO3- |
设NA为阿伏伽德罗常数,下列说法正确的是( )
| A、电解精炼铜过程中,电路中每通过NA个电子,阳极溶解铜32g |
| B、1L 2mol/L的NH4CI溶液中含NH4+数目为2NA |
| C、5.6g铁粉与硝酸反应失去的电子数一定为0.3NA |
| D、1molC20H42的分子中含有的共价键数目为61NA |
已知NA为阿伏伽德罗常数,下列说法不正确的是( )
| A、醋酸的摩尔质量与NA个醋酸分子的质量当以克为单位时在数值上相等 |
| B、22g二氧化碳与11.2L的HCl含有相同的分子数 |
| C、常温常压下,17gNH3所含有的原子数为4NA |
| D、500mL 0.2mol?L-1的Ba(NO3)2溶液中NO3-的物质的量浓度为0.4mol?L-1 |
将Fe片和Al片放在盛有NaCl溶液(其中滴入酚酞)的表面皿中,如图表示,最先观察到变红色的区域为( )
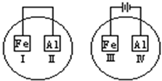

| A、II和Ⅳ | B、Ⅱ和Ⅲ |
| C、Ⅰ和Ⅲ | D、Ⅰ和Ⅳ |