题目内容
为了探究HClO的漂白性,某同学设计了如下的实验.
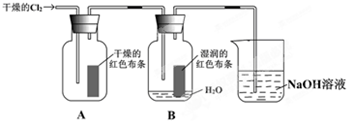
(1)写出C12与水反应的化学方程式
(2)通入C12后,集气瓶A中的现象是 ,集气瓶B中的现象是 ,可得出的结论是 .烧杯中的NAOH溶液的作用是 ,其反生反应的离子方程式为 .

(1)写出C12与水反应的化学方程式
(2)通入C12后,集气瓶A中的现象是
考点:氯、溴、碘及其化合物的综合应用,实验装置综合
专题:实验题
分析:(1)根据氯气和水反应的产物是盐酸和次氯酸;
(2)氯气能使湿润的有色布条褪色,但是不能使干燥的有色布条褪色,次氯酸具有漂白性,氯气没有漂白性;氯气有毒,可以用氢氧化钠来吸收.
(2)氯气能使湿润的有色布条褪色,但是不能使干燥的有色布条褪色,次氯酸具有漂白性,氯气没有漂白性;氯气有毒,可以用氢氧化钠来吸收.
解答:
解:(1)氯气和水反应生成的次氯酸具有漂白性,反应的化学方程式为:Cl2+H2O=HCl+HClO,故答案为:Cl2+H2O=HCl+HClO;
(2)通入C12后,干燥的氯气没有漂白性,集气瓶A中的现象是有色布条不褪色,集气瓶B中的现象是有色布条褪色,氯气能使湿润的有色布条褪色,干燥的氯气没有漂白性;氯水中次氯酸具有漂白性;氯气有毒,会造成空气污染,可以用氢氧化钠来吸收,反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:有色布条不褪色;红色布条褪色;干燥的氯气没有漂白性,次氯酸具有漂白性;吸收多余的氯气;Cl2+2OH-=Cl-+ClO-+H2O.
(2)通入C12后,干燥的氯气没有漂白性,集气瓶A中的现象是有色布条不褪色,集气瓶B中的现象是有色布条褪色,氯气能使湿润的有色布条褪色,干燥的氯气没有漂白性;氯水中次氯酸具有漂白性;氯气有毒,会造成空气污染,可以用氢氧化钠来吸收,反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:有色布条不褪色;红色布条褪色;干燥的氯气没有漂白性,次氯酸具有漂白性;吸收多余的氯气;Cl2+2OH-=Cl-+ClO-+H2O.
点评:本题考查HClO的漂白性的探究,题目难度不大,本题注意氯气与次氯酸性质的差异性,注意相关反应化学方程式或者离子方程式的书写.

练习册系列答案
相关题目
下列说法正确的是( )
| A、氧化还原反应的本质是反应前后有元素化合价的升降 |
| B、Ag++Cl-=AgCl↓ 的反应属于化合反应 |
| C、从1 L 1 mol/L的H2SO4溶液中取出10 mL该溶液,其中H+浓度为2 mol/L |
| D、晶体硅是制造光导纤维的原料 |
酚醛树脂可用苯酚和甲醛反应制得.实验室制备酚醛树脂时,在酸性条件下,苯酚过量制得酚醛树脂若不易取出,则可趁热时加入一些乙醇来取出酚醛树脂;在碱性条件下,苯酚过量时,若酚醛树脂不易取出时,用加热或加溶剂的方法都很难将酚醛树脂取出.在上述两种情况下,下列有关叙述正确的是( )
| A、酸性条件制得的是体型结构酚醛树脂,碱性条件制得的是线型结构酚醛树脂 |
| B、酸性条件制得的是线型结构酚醛树脂,碱性条件制得的是网状结构酚醛树脂 |
| C、两种条件下制得的都是线型结构的酚醛树脂 |
| D、两种条件下制得的都是网状结构酚醛树脂 |
下列说法不正确的是( )
| A、Mg的金属性比Al强 |
| B、H2S的热稳定性比H2O强 |
| C、Na的原子半径比N原子大 |
| D、HClO4的酸性比H3PO4强 |
