题目内容
8.对于A2+3B2=2C的反应来说,以下化学反应速率的表示中,反应速率最快的是( )| A. | V(B2)=0.8 mol/(L•s) | B. | V(A2)=0.8 mol/(L•s) | ||
| C. | V(C)=0.6 mol/(L•s) | D. | V(A2)=1.8 mol/(L•min) |
分析 不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,注意单位保持一致.
解答 解:不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快.
A.$\frac{v({B}_{2})}{3}$=0.267 mol/(L•s);
B.$\frac{v({A}_{2})}{1}$=0.8 mol/(L•s);
C.$\frac{v(C)}{2}$=0.3 mol/(L•s);
D.$\frac{v({A}_{2})}{1}$=1.8 mol/(L•min)=0.03 mol/(L•s);
故反应速率B>C>A>D,
故选:B.
点评 本题考查化学反应速率快慢比较,利用比值法可以迅速判断,也可以转化为同一物质表示想速率进行比较,注意保持单位一致.

练习册系列答案
相关题目
19.元素周期表是学习化学的重要工具,它隐含着许多信息和规律.下表所列是几种短周期元素的原子半径及主要化合价:
(1)用元素符号标出A、C、D、F在元素周期表中的相应位置(以下为元素周期表的一部分).
(2)A元素处于周期表中三周期IIA族.
(3)写出D离子的结构示意图 .
.
(4)上述A~F六种元素最高价氧化物对应水化物中酸性最强的是HClO4(填化学式).
(5)C元素气态氢化物的电子式为 .它与C元素最高价氧化物水化物反应的生成物是属于离子(离子或共价)化合物,其中含有的化学键类型有离子键、共价键.
.它与C元素最高价氧化物水化物反应的生成物是属于离子(离子或共价)化合物,其中含有的化学键类型有离子键、共价键.
(6)B的最高价氧化物的水化物与E的最高价氧化物的水化物反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
(7)元素E与元素F对比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是CD(填选项字母).
A.气态氢化物水溶液的酸性 B.气态氢化物的沸点
C.单质与氢气反应的难易程度 D.气态氢化物的稳定性.
| 元素(或元 素代码) | 铍 | A | B | C | D | E | F |
| 原子半径 (10-10m) | 0.89 | 1.60 | 1.43 | 0.75 | 0.74 | 1.02 | 0.99 |
| 最高价态 | +2 | +2 | +3 | +5 | - | +6 | +7 |
| 最低价态 | - | - | - | -3 | -2 | -2 | -1 |
(2)A元素处于周期表中三周期IIA族.
(3)写出D离子的结构示意图
 .
.(4)上述A~F六种元素最高价氧化物对应水化物中酸性最强的是HClO4(填化学式).
(5)C元素气态氢化物的电子式为
 .它与C元素最高价氧化物水化物反应的生成物是属于离子(离子或共价)化合物,其中含有的化学键类型有离子键、共价键.
.它与C元素最高价氧化物水化物反应的生成物是属于离子(离子或共价)化合物,其中含有的化学键类型有离子键、共价键.(6)B的最高价氧化物的水化物与E的最高价氧化物的水化物反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
(7)元素E与元素F对比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是CD(填选项字母).
A.气态氢化物水溶液的酸性 B.气态氢化物的沸点
C.单质与氢气反应的难易程度 D.气态氢化物的稳定性.
16.如表各组物质中,物质之间不可能实现如图所示转化的是( )
X$\stackrel{M}{→}$Y$\stackrel{M}{→}$Z
X$\stackrel{M}{→}$Y$\stackrel{M}{→}$Z
| 选项 | X | Y | Z | M |
| A | H2S | S | SO3 | O2 |
| B | Mg | C | CO | CO2 |
| C | NaOH | Na2CO3 | NaHCO3 | CO2 |
| D | NH3 | NO | NO2 | O2 |
| A. | A | B. | B | C. | C | D. | D |
3.某烃的分子式为C10H14,不能使溴水褪色,但可使酸性高锰酸钾溶液褪色,分子结构中只含有一个烷基,则此烷基的结构共有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
13.同质量的锌与盐酸反应,欲使反应速率增大,选用的反应条件正确的组合是( )
①锌粒
②锌片
③锌粉
④5%的盐酸
⑤10%的盐酸
⑥15%的盐酸
⑦加热
⑧用冷水冷却
⑨不断振荡
⑩迅速混合后静置.
①锌粒
②锌片
③锌粉
④5%的盐酸
⑤10%的盐酸
⑥15%的盐酸
⑦加热
⑧用冷水冷却
⑨不断振荡
⑩迅速混合后静置.
| A. | ②⑥⑦⑩ | B. | ①④⑧⑩ | C. | ③⑤⑦⑨ | D. | ③⑥⑦⑨ |
17.根据下列实验的操作和现象,可以得出正确结论的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向滴加有KSCN的FeCl2溶液,不断滴加氯水 | 溶液颜色先变红后褪色 | Fe2+先是被氧化为Fe3+,后来又被还原为Fe2+ |
| B | 向浓盐酸中加入少量碳酸钠溶液,将产生的气体通入苯酚钠溶液 | 苯酚钠溶液中出现白色浑浊 | 实验有缺陷,不能证明酸性:盐酸>碳酸>苯酚 |
| C | 在酸性KMnO4溶液中通入SO2 | 溶液褪色 | SO2具有漂白性 |
| D | 用标准浓度的烧碱溶液滴定未知浓度的盐酸,酚酞做指示剂 | 锥形瓶内溶液颜色由无色变为浅红色立即停止滴定 | 酸碱恰好中和 |
| A. | A | B. | B | C. | C | D. | D |
15.某中性有机物(分子式为C10H20O2)在稀硫酸作用下加热得到M和N两种有机物,且M被酸性KMnO4溶液作用可直接得到N.下列说法正确的是( )
| A. | M的分子式为C5H10O | |
| B. | 该中性有机物有4种(不考虑立体异构) | |
| C. | 上述过程发生的所有反应与油脂化反应的反应类型相同 | |
| D. | M和N都可以发生取代反应、都能与Na反应生成H2,因此具有相同官能团 |
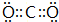 ;元素Z的离子结构示意图为
;元素Z的离子结构示意图为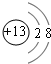 .
.