题目内容
19.元素周期表是学习化学的重要工具,它隐含着许多信息和规律.下表所列是几种短周期元素的原子半径及主要化合价:| 元素(或元 素代码) | 铍 | A | B | C | D | E | F |
| 原子半径 (10-10m) | 0.89 | 1.60 | 1.43 | 0.75 | 0.74 | 1.02 | 0.99 |
| 最高价态 | +2 | +2 | +3 | +5 | - | +6 | +7 |
| 最低价态 | - | - | - | -3 | -2 | -2 | -1 |
(2)A元素处于周期表中三周期IIA族.
(3)写出D离子的结构示意图
 .
.(4)上述A~F六种元素最高价氧化物对应水化物中酸性最强的是HClO4(填化学式).
(5)C元素气态氢化物的电子式为
 .它与C元素最高价氧化物水化物反应的生成物是属于离子(离子或共价)化合物,其中含有的化学键类型有离子键、共价键.
.它与C元素最高价氧化物水化物反应的生成物是属于离子(离子或共价)化合物,其中含有的化学键类型有离子键、共价键.(6)B的最高价氧化物的水化物与E的最高价氧化物的水化物反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
(7)元素E与元素F对比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是CD(填选项字母).
A.气态氢化物水溶液的酸性 B.气态氢化物的沸点
C.单质与氢气反应的难易程度 D.气态氢化物的稳定性.
分析 由于A的最高正价为+2,无最低负价,故和铍同一主族,故为Mg;B的最高正价为+3价,且半径比Mg小,比铍大,故为Al;C的最高正价为+5价,最低负价为-3价,且半径比铍还小,故为第二周期的N;D的最低负价为-2价,无最高正价,且半径比铍小,故为O;E的最高正价为+6,最低负价为-2价,故和O同为第VIA族,故为S;F的最高正价为+7,最低负价为-1价,故为第VIIA族,且由于原子半径比铍大,故为Cl.
(1)根据A为Mg、C为N、D为O、F为Cl来分析在周期表中的位置;
(2)A为Mg,原子核外有3个电子层,最外层有2个电子;
(3)D离子为O2-,核外有10个电子,核内有8个质子;
(4)元素的非金属性越强,则最高价含氧酸的酸性越强;
(5)C元素气态氢化物为NH3,最高价氧化物水化物为硝酸,两者反应生成硝酸铵,硝酸铵为离子化合物,结构中含离子键和共价键;
(6)B的最高价氧化物的水化物为氢氧化铝,E的最高价氧化物的水化物为硫酸,两者发生酸碱中和;
(7)同一周期的元素从左到右,非金属性逐渐增强,且非金属性越强,单质和氢气化合越容易,得到的气态氢化物越稳定,据此分析.
解答 解:由于A的最高正价为+2,无最低负价,故和铍同一主族,故为Mg;B的最高正价为+3价,且半径比Mg小,比铍大,故为Al;C的最高正价为+5价,最低负价为-3价,且半径比铍还小,故为第二周期的N;D的最低负价为-2价,无最高正价,且半径比铍小,故为O;E的最高正价为+6,最低负价为-2价,故和O同为第VIA族,故为S;F的最高正价为+7,最低负价为-1价,故为第VIIA族,且由于原子半径比铍大,故为Cl.
(1)由于A为Mg,处于第三周期、第IIA族;C为N,处于第二周期第VA族;D为O,处于第二周期第VIA族;F为Cl,处于第三周期第VIIA族,故可标出其在周期表中的位置,故答案为:
| N | O | ||||||||||||||||
| Mg | Cl | ||||||||||||||||
(2)A为Mg,原子核外有3个电子层,最外层有2个电子,故A在周期表中的位置为第三周期第IIA族,故答案为:三,ⅡA;
(3)D离子为O2-,核外有10个电子,核内有8个质子,故结构示意图为
 ,故答案为:
,故答案为: ;
;(4)元素的非金属性越强,则最高价含氧酸的酸性越强,而上述A~F六种元素中非金属性最强的为Cl,故其最高价含氧酸HClO4的酸性最强,故答案为:HClO4;
(5)C元素气态氢化物为NH3,电子式为:
 ,最高价氧化物水化物为硝酸,两者反应生成硝酸铵,而硝酸铵属于铵盐,为离子化合物,结构中含离子键和共价键,故答案为:
,最高价氧化物水化物为硝酸,两者反应生成硝酸铵,而硝酸铵属于铵盐,为离子化合物,结构中含离子键和共价键,故答案为: ;离子;离子键、共价键;
;离子;离子键、共价键;(6)B的最高价氧化物的水化物为氢氧化铝,E的最高价氧化物的水化物为硫酸,两者发生酸碱中和,离子方程式为:Al(OH)3+3H+=Al3++3H2O,故答案为:Al(OH)3+3H+=Al3++3H2O;
(7)同一周期的元素从左到右,非金属性逐渐增强,故Cl的非金属性强于S;且非金属性越强,单质和氢气化合越容易,得到的气态氢化物越稳定,但对氢化物溶于水后的酸性和沸点无关,故答案为:Cl;CD.
点评 本题考查学生元素周期表中元素分布以及元素周期律的知识,可以根据所学知识来回答,难度不大.

 名校课堂系列答案
名校课堂系列答案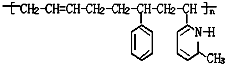 新弹性材料丁基苯呲橡胶可通过加聚反应得到,其结构简式如图,其单体可能是以下物质中的某几种,则正确的一组单体是( )
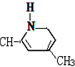
新弹性材料丁基苯呲橡胶可通过加聚反应得到,其结构简式如图,其单体可能是以下物质中的某几种,则正确的一组单体是( )①CH2=CH-CH2-CH3
②CH2=
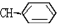
③CH2=CH-CH=CH2
④CH3-CH=CH-CH3
⑤CH2=CH-
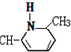
⑥CH2=CH-
| A. | ①②⑥ | B. | ②③⑤ | C. | ①②⑤ | D. | ②④⑥ |
| A. | KCl(NH4Cl)用加热法分离 | B. | CO2(SO2)通过饱和的碳酸钠溶液洗气 | ||
| C. | NO(NO2)通过水洗气 | D. | FeCl3溶液(FeCl2)通入氯气 |
| A. | 澄清石灰水 | B. | 盐酸酸化的Ba(NO3)2溶液 | ||
| C. | BaCl2溶液 | D. | BaCl2与NaOH的混合溶液 |
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O CO2 | ||
| C. | NH3 H2O CO2 | D. | CaCl2 NaOH H2 |
| A. | V(B2)=0.8 mol/(L•s) | B. | V(A2)=0.8 mol/(L•s) | ||
| C. | V(C)=0.6 mol/(L•s) | D. | V(A2)=1.8 mol/(L•min) |
| A. | S+O2 $\frac{\underline{\;\;△\;\;}}{\;}$ SO2 | B. | 4FeS2+11O2 $\frac{\underline{\;高温\;}}{\;}$ 2Fe2O3+8SO2 | ||
| C. | 2SO2+O2 $?_{加热}^{催化剂}$ 2SO3 | D. | SO3+H2O=H2SO4 |