题目内容
13.同质量的锌与盐酸反应,欲使反应速率增大,选用的反应条件正确的组合是( )①锌粒
②锌片
③锌粉
④5%的盐酸
⑤10%的盐酸
⑥15%的盐酸
⑦加热
⑧用冷水冷却
⑨不断振荡
⑩迅速混合后静置.
| A. | ②⑥⑦⑩ | B. | ①④⑧⑩ | C. | ③⑤⑦⑨ | D. | ③⑥⑦⑨ |
分析 用锌粒与稀盐酸反应制取氢气时,增大氢离子的浓度、升高温度、增大接触面积等可加快反应速率,以此来解答.
解答 解:①锌粒 ②锌片 ③锌粉相比较,锌粉表面积最大,反应速率最大;
④5%盐酸 ⑤10%盐酸 ⑥15%盐酸相比较,⑥浓度最大,反应速率最大;
⑦加热 ⑧用冷水冷却 相比较,升高温度反应速率增大;
混合后,无需搅拌,静置可迅速反应,③⑥⑦⑨可以使反应速率增大.
故选D.
点评 本题考查影响化学反应速率的因素,明确温度、浓度、催化剂对反应的影响即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
8.对于A2+3B2=2C的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
| A. | V(B2)=0.8 mol/(L•s) | B. | V(A2)=0.8 mol/(L•s) | ||
| C. | V(C)=0.6 mol/(L•s) | D. | V(A2)=1.8 mol/(L•min) |
18.为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施.化学反应的焓变通常用实验进行测定,也可进行理论推算.
(1)实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452.8kJ/mol.
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.已知反应N2(g)+3H2(g)?2NH3(g)△H=akJ•mol-1.试根据表中所列键能数据计算a的数值-93:
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(石墨,s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1①
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1②
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1③
根据盖斯定律,298K时由C(石墨,s)和H2(g)生成C2H2(g)反应的热化学方程式:2C (s,石墨)+H2(g)=C2H2(g)△H=+226.7kJ•mol-1.
(1)实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452.8kJ/mol.
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.已知反应N2(g)+3H2(g)?2NH3(g)△H=akJ•mol-1.试根据表中所列键能数据计算a的数值-93:
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 945 |
已知:C(石墨,s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1①
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1②
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1③
根据盖斯定律,298K时由C(石墨,s)和H2(g)生成C2H2(g)反应的热化学方程式:2C (s,石墨)+H2(g)=C2H2(g)△H=+226.7kJ•mol-1.
5.某课外活动小组同学用如图装置进行实验,下列有关说法中,正确的是( )
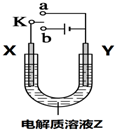

| A. | 若X、Y、Z分别为铁片、铜片、氯化铜溶液,开关K与a连接,则Y极上有气泡放出 | |
| B. | 若X、Y、Z分别为铁片、铜片、氯化铜溶液,开关K与a连接,则溶液中Cu2+向Y极移动 | |
| C. | 若X、Y、Z分别为石墨、石墨、氯化铜溶液,开关K与b连接,则溶液中Cu2+向Y极移动 | |
| D. | 若X、Y、Z分别为石墨、石墨、氯化铜溶液,开关K与b连接,则 Y极上有黄绿色气体生成 |
2.镁铝合金(Mg17Al12)是一种潜在的储氢材料,该合金在一定条件下完全吸氢的化学方程式为Mg17Al12+17H2═12Al+17MgH2.得到的混合物G(12Al+17MgH2).0.1molG和足量的稀盐酸反应放出的H2与O2在KOH溶液中构成燃料电池,理论上正极上消耗氧气体积(标准状况)为( )
| A. | 44.80L | B. | 58.24L | C. | 80.64L | D. | 116.48L |
20.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 22.4L O2的分子数约为NA | |
| B. | 标准状况下,11.2L H2O的分子数约为0.5NA | |
| C. | 1 L 1mol/L的NaOH溶液中Na+的数目为NA | |
| D. | 0.1mol铁与足量的盐酸完全反应,铁失去的电子数为0.1NA |
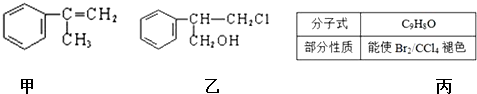
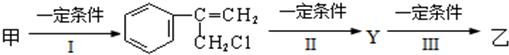
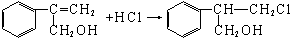 (不需注明反应条件).
(不需注明反应条件).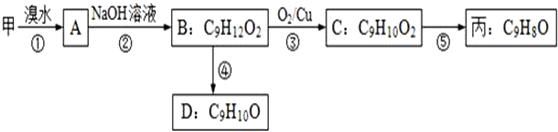
 .
. 、
、