题目内容
3.将20mLNO2和NH3的混合气体,在一定条件下充分反应,化学方程式是:6NO2+8NH3═7N2+12H2O.已知参加反应的NO2比参加反应的NH3少2mL(气体体积均在相同状况下测定),则原混合气体中NO2和NH3的物质的量之比是( )| A. | 3:2 | B. | 2:3 | C. | 3:5 | D. | 3:4 |
分析 实际参加反应的NO2比NH3少2mL,由6NO2+8NH3=7N2+12H2O可知,参加反应的NO2、NH3的体积分别为6mL、8mL,故剩余气体为20mL-6mL-8mL=6mL,剩余气体可能为NO2,可能为NH3,据此讨论计算.
解答 解:实际参加反应的NO2比NH3少2mL,由6NO2+8NH3=7N2+12H2O可知,参加反应的NO2、NH3的体积分别为6mL、8mL,则剩余气体为20mL-6mL-8mL=6mL,
若剩余气体为NO2,则V(NO2)=6mL+6mL=12mL,物质的量之比等于体积之比,故n(NO2):n(NH3)=V(NO2):v(NH3)=12mL:8mL=3:2,
若剩余气体为NH3,则v(NH3)=8mL+6mL=14mL,物质的量之比等于体积之比,故n(NO2):n(NH3)=V(NO2):v(NH3)=6mL:14mL=3:7,
根据分析可知,正确的为A,
故选A.
点评 本题考查氧化还原反应的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握讨论法在化学计算中的应用,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
9.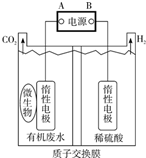 在微生物作用下电解有机废水(含CH3COOH),可获得清洁能源H2,其原理如图所示,下列有关说法不正确的是( )
在微生物作用下电解有机废水(含CH3COOH),可获得清洁能源H2,其原理如图所示,下列有关说法不正确的是( )
 在微生物作用下电解有机废水(含CH3COOH),可获得清洁能源H2,其原理如图所示,下列有关说法不正确的是( )
在微生物作用下电解有机废水(含CH3COOH),可获得清洁能源H2,其原理如图所示,下列有关说法不正确的是( )| A. | 电极B极为负极 | |
| B. | 与电源A极相连的惰性电极上发生的反应为:CH3COOH-8e-+H2O=2CO2↑+8H+ | |
| C. | 通电后,H+通过质子交换膜向右移动,最终右侧溶液pH减小 | |
| D. | 通电后,若有0.1molH2生成,则转移0.2mol电子 |
14.利用如图所示装置可制取 H2,两个电极均为惰性电极,c 为阴离子交换膜.下列叙述正确的是( )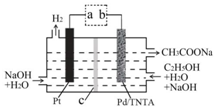

| A. | a 为电源的正极 | |
| B. | 工作时,OH-向左室迁移 | |
| C. | 右室电极反应为:C2H5OH+H2O-4e-═CH3COO-+5H+ | |
| D. | 生成 H2 和 CH3COONa 的物质的量之比为 2:1 |
11.下列关于有机化合物的说法正确的是( )
| A. | 1mol的  与足量的NaOH溶液反应,能消耗3mol NaOH 与足量的NaOH溶液反应,能消耗3mol NaOH | |
| B. | 可用氢氧化钠溶液除去乙酸乙酯中残留的乙酸 | |
| C. | 间二甲苯也叫1,5-二甲苯 | |
| D. | 乙二醇和丙三醇互为同系物 |
15.柠檬酸是常见的食品添加剂,其结构式如图所示.以下叙述正确的是( )


| A. | 柠檬酸分子式为C6H9O7 | |
| B. | 使用食品添加剂属于违法行为 | |
| C. | 柠檬酸可用作食品抗氧化剂,说明其有较强氧化性 | |
| D. | 柠檬酸分子含三个羧基(-COOH) |
12.下列离子反应方程式正确的是( )
| A. | 少量二氧化碳通入“水玻璃”中:CO2+SiO32-+H2O═CO32-+H2SiO3↓ | |
| B. | 碳酸钙与稀盐酸混合:CO32-+2H+═CO2↑+H2O | |
| C. | 铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| D. | Al2O3溶于NaOH溶液中:Al2O3+2OH-═2[Al(OH)4]- |
13.在恒温恒容密闭容器中发生反应NH2COONH4(s)?2NH3(g)+CO2(g),不能判断该反应已达到化学平衡的是( )
| A. | 2v(NH3)=v(CO2) | |
| B. | 密闭容器中总压强不变 | |
| C. | 密闭容器中混合气体的密度不变 | |
| D. | 密闭容器中混合气体的平均摩尔质量不变 |
 $\stackrel{铑催化剂}{→}$
$\stackrel{铑催化剂}{→}$ (R1代表氢原子或烃基)
(R1代表氢原子或烃基)
 +
+ $\stackrel{碱}{→}$
$\stackrel{碱}{→}$ +H2O
+H2O .
. )是一种定香剂,以芳香醇A为原料合成H的一种流程如图:
)是一种定香剂,以芳香醇A为原料合成H的一种流程如图:
 +H2O(R1、R表示氢原子或烃基)
+H2O(R1、R表示氢原子或烃基) ;H的官能团名称是碳碳双键、酯基.
;H的官能团名称是碳碳双键、酯基. .
. (写一种即可).
(写一种即可).