题目内容
20.(1)表中有三组物质,每组均有甲、乙、丙三种物质(酸、碱、盐均为溶液).| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 甲 | BaCl2 | HCl | Cu(NO3)2 |
| 乙 | Fe2O3 | K2SO4 | H2SO4 |
| 丙 | Fe | NaOH | NaHCO3 |
①第Ⅲ组中有一种物质能与第Ⅰ组中的所有物质反应,这种物质是H2SO4.
②第Ⅱ组物质中,跟第Ⅰ组所有物质都不能发生反应的是NaOH,该物质能与第Ⅲ组中所有物质发生反应,其离子反应方程式分别为:Cu2++2OH-=Cu(OH)2↓,OH-+H+=H2O,OH-+HCO3-=CO32-+H2O.
( 2)现有下列几种物质
①铜 ②稀硫酸 ③氯化氢 ④氯气 ⑤空气 ⑥二氧化碳 ⑦盐酸 ⑧氯化钠 ⑨熔融的硝酸钾 ⑩硫酸钡
其中,属于混合物的有②⑤⑦,( 填序号,下同)属于电解质的有③⑧⑨⑩,属于非电解质的有⑥.
分析 (1)①硫酸与氯化钡反应生成硫酸钡沉淀和盐酸,硫酸与氧化铁反应生成硫酸铁和水,硫酸与铁反应生成硫酸亚铁和氢气,依此进行判断;
②氢氧化钠与氯化钡、氧化铁、铁都不反应;氢氧化钠与硝酸铜反应生成氢氧化铜沉淀和硝酸钠,氢氧化钠与硫酸反应生成硫酸钠和水,氢氧化钠与碳酸氢钠反应生成碳酸钠和水;
(2)有两种以上物质组成的物质属于混合物;只有一种物质组成的是纯净物,包括单质、化合物;
在水溶液里或熔融状态下能导电的化合物是电解质,包括酸、碱、盐、活泼金属氧化物和水;
在水溶液里和熔融状态下都不能导电的化合物是非电解质,包括一些非金属氧化物、氨气、大多数有机物(如蔗糖、酒精等).
解答 解:(1)①硫酸与氯化钡反应生成硫酸钡沉淀和盐酸,硫酸与氧化铁反应生成硫酸铁和水,硫酸与锌反应生成硫酸锌和氢气,故第Ⅲ组中的H2SO4能与第Ⅰ组中的所有物质反应,
故答案为:Ⅰ;H2SO4;
②氢氧化钠与氯化钡、氧化铁、锌都不反应;氢氧化钠与硝酸铜反应生成氢氧化铜沉淀和硝酸钠,方程式为:Cu2++2OH-=Cu(OH)2↓,氢氧化钠与硫酸反应生成硫酸钠和水,方程式为:OH-+H+=H2O,氢氧化钠与碳酸氢钠反应生成碳酸钠和水,方程式为:OH-+HCO3-=CO32-+H2O,
故答案为:NaOH;Cu2++2OH-=Cu(OH)2↓; OH-+H+=H2O; OH-+HCO3-=CO32-+H2O;
(2)①铜是单质,是纯净物;含有自由电子,能够导电;既不是电解质,也不是非电解质;
②稀硫酸含有硫酸和水分子,属于混合物;含有自由离子,能导电;既不是电解质,也不是非电解质;
③氯化氢属于化合物,属于纯净物;不含自由电子和离子,不能导电;在水溶液里能够完全电离产生自由移动的离子而导电,属于强电解质;
④氯气属于化合物,属于纯净物;为单质,既不是电解质也不是非电解质;
⑤空气属于混合物,不含自由电子和离子,不能导电;既不是电解质,也不是非电解质;
⑥二氧化碳属于化合物,属于纯净物;不含自由电子和离子,不能导电;本身不能电离,属于非电解质;
⑦盐酸是氯化氢气体的水溶液属于混合物;含有自由电子,能够导电;既不是电解质,也不是非电解质;
⑧氯化钠是化合物,属于纯净物;不含自由电子和离子,不能导电;在水溶液里能够完全电离产生自由移动的离子而导电,属于电解质;
⑨熔融硝酸钾是化合物,属于纯净物,含自由电子和离子能导电,属于电解质;
碳酸钙是化合物,属于纯净物;不含自由电子和离子,不能导电;在熔融状态下能够完全电离产生自由移动的离子而导电,属于强电解质;
⑩硫酸钡不溶于水,熔融状态下导电属于电解质;
故答案为:②⑤⑦;③⑧⑨⑩;⑥.
点评 本题考查物质的分类以及电解质、非电解质等知识,为高频考点,侧重于学生的分析的考查,注意把握相关概念的理解,难度不大.

| A. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 | |
| B. | 金属与酸的反应 | |
| C. | 甲烷在氧气中的燃烧反应 | |
| D. | 锌粒与稀硫酸的反应 |
 分子结构的下列叙述中,正确的是( )
分子结构的下列叙述中,正确的是( )| A. | 七个碳原子可能不在同一平面上 | B. | 具有单键和双键两种键 | ||
| C. | 八个氢原子不可能都在同一平面上 | D. | 最多可能有5个C原子在一条直线上 |
| A. | 取25 g CuSO4•5H2O溶于1 L水中 | |
| B. | 取16 g CuSO4•5H2O溶于少量水中,再稀释至1 L | |
| C. | 取16 g无水CuSO4溶于1 L水中 | |
| D. | 取25 g CuSO4•5H2O溶于水配成1 L溶液 |
| H2(g) | Br2(g) | HBr (g) | |
| 1mol分子中的化学键断裂时需吸收的能量(KJ) | 436 | a | 369 |
| A. | 404 | B. | 260 | C. | 230 | D. | 200 |
| A. | 溴水、FeCl3溶液 | B. | 溴水、酸性KMnO4溶液 | ||
| C. | 溴水、Na2CO3溶液 | D. | FeCl3溶液、酸性KMnO4溶液 |
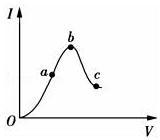 阅读下列信息,完成下列各题
阅读下列信息,完成下列各题