题目内容
3.下列关于相对原子质量的说法正确的是( )| A. | 是原子的实际质量 | B. | 是质子数加中子数 | ||
| C. | 标准是碳-12原子质量的$\frac{1}{12}$ | D. | 相对原子质量的单位是Kg |
分析 国际上是以一种碳原子的质量的$\frac{1}{12}$作为标准,其他原子的质量跟它相比较所得到的比值,就是该原子的相对原子质量;相对原子质量是一个比值,单位是“1”,常省略不写,据此进行分析判断.
解答 解:A.相对原子质量是原子的质量与碳原子质量的$\frac{1}{12}$的比值,故相对原子质量不是原子质量,故A错误;
B.由于相对原子质量是原子的质量与碳原子质量的$\frac{1}{12}$的比值,该比值约等于原子中质子数和中子数之和,故B错误;
C.国际上是以一种碳原子的质量的$\frac{1}{12}$作为标准,其他原子的质量跟它相比较所得到的比值,故C正确;
D.相对原子质量的单位是1,故D错误;
故选:C.
点评 本题考查了相对原子质量的理解,熟悉相对原子质量概念、单位是解题关键,题目难度不大.

练习册系列答案
相关题目
13.下列电子式书写正确的是( )
| A. | N2:N:::N: | B. | NH3  | C. | H2O  | D. | KOH  |
14.下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A. | pH相同的①CH3COONa②NaHCO3③NaClO三份溶液中的c(Na+):②>③>① | |
| B. | 将0.5mol/L的Na2CO3溶液与amol/L的NaHCO3溶液等体积混合,c(Na+)<c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | 10mL0.1mol/LCH3COOH溶液与20mL0.1mol/LNaOH溶液混合后,溶液中离子浓度关系为:c(OH-)=c(CH3COO-)+2c(CH3COOH) | |
| D. | 25℃某浓度的NaCN溶液的pH=d,则其中又水电离出的c(OH-)=10-dmol/L |
11.能与Fe3+反应,且反应中Fe3+起氧化作用的是( )
①SCN- ②Fe ③Fe2+ ④Cu ⑤I- ⑥OH-.
①SCN- ②Fe ③Fe2+ ④Cu ⑤I- ⑥OH-.
| A. | ①②⑤ | B. | ①③⑥ | C. | ①②③ | D. | ②④⑤ |
15.碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应生成的气体Y同时通入盛有足量BaCl2溶液的洗气瓶,下列有关说法不正确的是( )
| A. | 洗气瓶中产生的沉淀是BaCO3 | B. | 最终导出的气体中有CO2 | ||
| C. | 洗气瓶中产生的沉淀是BaSO4 | D. | 最终导出的气体可能是红棕色的 |
6.将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述错误的是( )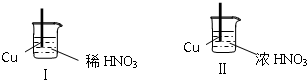
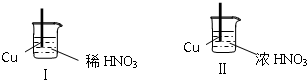
| A. | 两个反应产生的气体不同 | |
| B. | Ⅱ比Ⅰ的反应速率快的原因是因为反应物浓度大 | |
| C. | 浓硝酸在常温下和不同金属反应的现象可能不同 | |
| D. | 浓硝酸与铜反应降价少,所以浓硝酸的氧化性弱 |
7.已知:H2CO3的酸性大于HClO,HClO的酸性大于HCO3-的酸性,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| A. | c(HCO3-)>c(ClO-)>c(OH-) | B. | c(ClO-)>c(HCO3-)>c(H+) | ||
| C. | c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) | D. | c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-) |
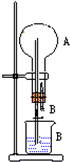 在图装置中,烧瓶中充满干燥气体A,将滴管中的液体B挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹,尖嘴管有液体呈喷泉状喷出,最终几乎充满烧瓶.
在图装置中,烧瓶中充满干燥气体A,将滴管中的液体B挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹,尖嘴管有液体呈喷泉状喷出,最终几乎充满烧瓶.