题目内容
现有由等质量的NaHCO3和KHCO3组成的混合物a g,与100mL盐酸反应.(题中涉及的气体体积均以标准状况计,填空时可以用带字母的式子表示)
(1)该混合物中NaHCO3与KHCO3的物质的量之比为 ;
(2)如碳酸氢盐与盐酸恰好完全反应,则盐酸中HCl的物质的量的计算式为 mol;(不需要化简)
(3)如果盐酸过量,生成CO2的体积的计算式为 L;(不需要化简)
(4)如果反应后碳酸氢盐有剩余,盐酸不足量,要计算生成CO2的体积,还需要知道 ;
(5)若NaHCO3和KHCO3不是以等质量混合,则a g固体混合物与足量的盐酸完全反应时生成CO2的体积[V(CO2)]范围是 .(不需要化简)
(1)该混合物中NaHCO3与KHCO3的物质的量之比为
(2)如碳酸氢盐与盐酸恰好完全反应,则盐酸中HCl的物质的量的计算式为
(3)如果盐酸过量,生成CO2的体积的计算式为
(4)如果反应后碳酸氢盐有剩余,盐酸不足量,要计算生成CO2的体积,还需要知道
(5)若NaHCO3和KHCO3不是以等质量混合,则a g固体混合物与足量的盐酸完全反应时生成CO2的体积[V(CO2)]范围是
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:(1)根据n=
计算;
(2)NaHCO3和KHCO3组成的混合物与盐酸恰好反应,由HCO3-+H+=CO2↑+H2O,可知n(HCl)=n(NaHCO3)+(KHCO3);
(3)根据碳元素守恒可知,n(CO2)=n(NaHCO3)+(KHCO3),再根据V=nVm计算生成的二氧化碳的体积;
(4)碳酸氢盐与盐酸按1:1反应,盐酸不足量,碳酸氢盐有剩余,应根据HCl的物质的量计算二氧化碳的体积;
(5)假定碳酸氢盐全是NaHCO3,根据碳元素守恒计算生成二氧化碳的物质的量,假定碳酸氢盐全是KHCO3,根据碳元素守恒计算生成二氧化碳的物质的量,实际二者生成二氧化碳的物质的量之间,进而确定体积范围.
| m |
| M |
(2)NaHCO3和KHCO3组成的混合物与盐酸恰好反应,由HCO3-+H+=CO2↑+H2O,可知n(HCl)=n(NaHCO3)+(KHCO3);
(3)根据碳元素守恒可知,n(CO2)=n(NaHCO3)+(KHCO3),再根据V=nVm计算生成的二氧化碳的体积;
(4)碳酸氢盐与盐酸按1:1反应,盐酸不足量,碳酸氢盐有剩余,应根据HCl的物质的量计算二氧化碳的体积;
(5)假定碳酸氢盐全是NaHCO3,根据碳元素守恒计算生成二氧化碳的物质的量,假定碳酸氢盐全是KHCO3,根据碳元素守恒计算生成二氧化碳的物质的量,实际二者生成二氧化碳的物质的量之间,进而确定体积范围.
解答:
解:等质量的NaHCO3和KHCO3组成的混合物a g,
(1)该混合物中NaHCO3与KHCO3的物质的量之比为
:
=100:84,故答案为:100:84;
(2)NaHCO3的物质的量=
=
mol,KHCO3的物质的量=
=
mol,混合物与100mL盐酸恰好反应,碳酸氢盐与盐酸按1:1反应,则n(HCl)=n(NaHCO3)+(KHCO3)=
mol+
mol=
mol,故答案为:
;
(3)盐酸过量,NaHCO3和KHCO3组成的混合物完全反应,根据碳元素守恒可知,n(CO2)=n(NaHCO3)+(KHCO3)=
mol+
mol=(
+
)mol,所以标准状况下生成CO2的体积为=(
+
)mol×22.4L/mol=
L,
故答案为:
;
(4)碳酸氢盐与盐酸按1:1反应,盐酸不足量,碳酸氢盐有剩余,应根据HCl的物质的量计算二氧化碳的体积,所以要计算生成CO2的体积,还需要知道盐酸的物质的量浓度,
故答案为:盐酸的物质的量浓度;
(5)假定碳酸氢盐全是NaHCO3,则n(NaHCO3)=
=
mol,NaHCO3完全反应,根据碳元素守恒,可知生成二氧化碳n(CO2)=n(NaHCO3)═
mol;
假定碳酸氢盐全是KHCO3,则n(KHCO3)=
=
mol,KHCO3完全反应,根据碳元素守恒,可知生成二氧化碳n(CO2)=n(KHCO3)=
mol,所以实际二氧化碳的物质的量为
mol<n(CO2)<
mol,故标况下
L<V(CO2)<
L,
故答案为:
L<V(CO2)<
L.
(1)该混合物中NaHCO3与KHCO3的物质的量之比为
| ||
| 84g/mol |
| ||
| 100g/mol |
(2)NaHCO3的物质的量=
| ||
| 84g/mol |
| a |
| 168 |
| ||
| 100g/mol |
| a |
| 200 |
| a |
| 168 |
| a |
| 200 |
| 23a |
| 2100 |
| 23a |
| 2100 |
(3)盐酸过量,NaHCO3和KHCO3组成的混合物完全反应,根据碳元素守恒可知,n(CO2)=n(NaHCO3)+(KHCO3)=
| a |
| 168 |
| a |
| 200 |
| a |
| 168 |
| a |
| 200 |
| a |
| 168 |
| a |
| 200 |
| 23a×22.4 |
| 2100 |
故答案为:
| 23a×22.4 |
| 2100 |
(4)碳酸氢盐与盐酸按1:1反应,盐酸不足量,碳酸氢盐有剩余,应根据HCl的物质的量计算二氧化碳的体积,所以要计算生成CO2的体积,还需要知道盐酸的物质的量浓度,
故答案为:盐酸的物质的量浓度;
(5)假定碳酸氢盐全是NaHCO3,则n(NaHCO3)=
| ag |
| 84g/mol |
| a |
| 84 |
| a |
| 84 |
假定碳酸氢盐全是KHCO3,则n(KHCO3)=
| ag |
| 100g/mol |
| a |
| 100 |
| a |
| 100 |
| a |
| 100 |
| a |
| 84 |
| 22.4a |
| 100 |
| 22.4a |
| 84 |
故答案为:
| 22.4a |
| 100 |
| 22.4a |
| 84 |
点评:本题考查混合物的计算、根据方程式的计算等,题目属于字母型计算,增大计算难度,为易错题目,(5)中范围的计算,注意极限法的利用.

练习册系列答案
相关题目
为提纯下列物质(括号内的物质为为杂质),所选用的除杂试剂和分离方法都正确的是( )
| 被提纯物质 | 除杂试剂 | 分离方法 | |
| A | 苯(苯甲酸) | 生石灰 | 蒸馏 |
| B | 乙醇(乙酸) | 氢氧化钠溶液 | 分液 |
| C | 乙烷(乙炔) | 酸性高锰酸钾溶液 | 洗气 |
| D | 苯(苯酚) | 浓溴水 | 过滤 |
| A、A | B、B | C、C | D、D |
下列关于氯水的叙述正确的是( )
| A、新制氯水可使蓝色石蕊试纸先变红后褪色 |
| B、新制氯水中只含Cl2和H2O分子 |
| C、光照氯水有气泡放出,该气体主要是Cl2 |
| D、氯水放置数天后酸性将减弱 |
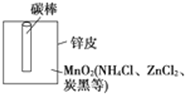 某学校设计了一节实验活动课,让学生从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质.整个实验过程如下,请回答有关问题:
某学校设计了一节实验活动课,让学生从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质.整个实验过程如下,请回答有关问题:

 A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,已知A为单质.写出A→E的化学式:
A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,已知A为单质.写出A→E的化学式: