题目内容
17.某物质有以下性质:①是电解质,②溶解时有化学键的破坏,③熔化时没有化学键的破坏,则该物质固态时属于( )| A. | 原子晶体 | B. | 分子晶体 | C. | 离子晶体 | D. | 金属晶体 |
分析 根据晶体中构成微粒以及微粒之间的作用力分析,分子晶体在熔化时不破坏化学键.
解答 解:已知某物质有以下性质:①是电解质 ②溶解时有化学键的破坏 ③熔化时没有化学键的破坏,
A.原子晶体在熔化时破坏共价键,破坏了化学键,故A不选;
B.分子晶体在熔化时不破坏化学键,如HCl,属于电解质,溶于水发生电离破坏化学键,熔化时没有化学键的破坏,故B选,
C.离子晶体在熔化时破坏离子键,破坏了化学键,故C不选.
D.金属晶体熔化时破坏金属键,破坏了化学键,故D不选.
故选B.
点评 本题考查了不同晶体的物理性质,题目难度不大,注意把握晶体的构成微粒和微粒间的作用力,侧重于考查学生的分析能力.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
8.向200mL 0.1mol/L 的Fe(NO3)2溶液中加入一定量NaOH,使Fe2+完全沉淀,过滤、加热并灼烧直至质量不再变化,此时固体的质量可能为( )
| A. | 1.60 g | B. | 2.76 g | C. | 4.36 g | D. | 5.54 g |
5.无铁硫酸铝是制造高档纸张和高级织物的重要原材料,制取无铁硫酸铝的工艺流程如图所示.铝土矿酸溶后得到含铁(Fe2+和Fe3+)的硫酸铝溶液,再经过后续加工,最终得到成品无铁硫酸铝(溶液中各种金属离子开始沉淀和沉淀完全时的pH见表).
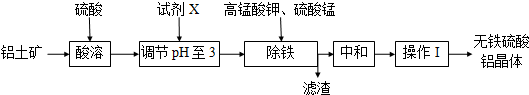
(1)试剂X可以用下列试剂中的a(填编号)
a.铝土矿粉 b.氢氧化钠 c.氧化钙
(2)生产中控制pH为3而不大于3的原因是pH超过3.3将导致Al3+沉淀,降低成品产量;
(3)操作I的名称蒸发浓缩、冷却结晶、过滤洗涤;
(4)除铁时,必须先加入高锰酸钾溶液,目的是把Fe2+转化为Fe3+;高锰酸钾溶液和硫酸锰溶液反应生成活性二氧化锰,写出反应的化学方程式2KMnO4+3MnSO4+2H2O═5MnO2↓+2H2SO4+K2SO4;
(5)滤渣的含铁成分是Fe(OH)3,用离子方程式表示其成因Fe3++3H2O?Fe(OH)3+3H+;
(6)活性二氧化锰能和Fe(OH)3发生吸附共沉作用,用化学平衡理论解释活性二氧化锰的作用吸附Fe(OH)3,促使Fe3+水解而充分沉淀(或促使水解平衡正向移动).

| 开始 | 完全 | |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.3 | 5.0 |
| Mn2+ | 8.3 | 9.8 |
a.铝土矿粉 b.氢氧化钠 c.氧化钙
(2)生产中控制pH为3而不大于3的原因是pH超过3.3将导致Al3+沉淀,降低成品产量;
(3)操作I的名称蒸发浓缩、冷却结晶、过滤洗涤;
(4)除铁时,必须先加入高锰酸钾溶液,目的是把Fe2+转化为Fe3+;高锰酸钾溶液和硫酸锰溶液反应生成活性二氧化锰,写出反应的化学方程式2KMnO4+3MnSO4+2H2O═5MnO2↓+2H2SO4+K2SO4;
(5)滤渣的含铁成分是Fe(OH)3,用离子方程式表示其成因Fe3++3H2O?Fe(OH)3+3H+;
(6)活性二氧化锰能和Fe(OH)3发生吸附共沉作用,用化学平衡理论解释活性二氧化锰的作用吸附Fe(OH)3,促使Fe3+水解而充分沉淀(或促使水解平衡正向移动).
12.根据表提供的数据,下列判断正确的是( )
| 化学式 | 电离常数 |
| HF | Ki=3.5×10-4 |
| H2CO3 | Ki1=4.4×10-7 |
| Ki2=4.7×10-11 | |
| HClO | Ki=3.2×10-8 |
| A. | 同温同浓度下,溶液的pH:NaF>NaClO>Na2CO3 | |
| B. | 结合H+的能力:ClO-<HCO3-<F- | |
| C. | 次氯酸钠溶液中通少量二氧化碳的离子方程式:ClO-+CO2+H2O═HCO3-+HClO | |
| D. | 碳酸钠溶液中加入少量氢氟酸的离子方程式:CO32-+2HF═2F-+H2O+CO2↑ |
2.分析如下残缺的反应:RO3-+□+6H+→3R2↑+3H2O.下列叙述正确的是( )
| A. | 上式中缺项所填物质在反应中作氧化剂 | |
| B. | 在RO3-参与的氧化还原反应中,R元素只能被还原 | |
| C. | 上述反应中,转移电子数为5NA | |
| D. | 同周期主族元素原子中R的原子半径最小 |
14.镧是重要的稀土元素,应用非常广泛,如应用于压电材料、催化剂等领域.

已知:
①镧是较活泼金属,在空气中易被氧化;
②氢氧化镧是难溶于水的弱碱;
③
(1)操作1、3是相同操作,其名称是过滤.
(2)操作2要在HCl气体的氛围内加热的原因是防止LaCl3水解.
(3)电解制镧的尾气要用碱液吸收,请写出反应的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
(4)真空、高温过程中的反应方程式为3Ca+2LaF3$\frac{\underline{\;真空\;}}{高温}$3CaF2+2La.
(5)粗镧精制过程中温度控制范围1487~3470℃.
(6)重熔蒸馏制得的镧中仍然混有极少量的钙.某批次产品69.709g,经分析含钙0.209g,该产品的等级为分析纯(化工产品等级标准:优级纯≥99.8%,分析纯≥99.7%,化学纯≥99.5%)

已知:
①镧是较活泼金属,在空气中易被氧化;
②氢氧化镧是难溶于水的弱碱;
③
| 金 属 | 熔点(℃) | 沸点(℃) |
| 钙 | 841 | 1 487 |
| 镧 | 920 | 3 470 |
(2)操作2要在HCl气体的氛围内加热的原因是防止LaCl3水解.
(3)电解制镧的尾气要用碱液吸收,请写出反应的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
(4)真空、高温过程中的反应方程式为3Ca+2LaF3$\frac{\underline{\;真空\;}}{高温}$3CaF2+2La.
(5)粗镧精制过程中温度控制范围1487~3470℃.
(6)重熔蒸馏制得的镧中仍然混有极少量的钙.某批次产品69.709g,经分析含钙0.209g,该产品的等级为分析纯(化工产品等级标准:优级纯≥99.8%,分析纯≥99.7%,化学纯≥99.5%)
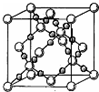 X、Y、Z、Q、R为原子序数依次增大的前四周期元素.X的一种1﹕2型氢化物分子中既有σ键又有π键,且分子中所有原子共平面;Z的L层有2个未成对电子;Q是所在周期中电负性最大的元素,QZ2可替代Q2作新的自来水消毒剂;R在周期表中位于d区,其基态原子有两个能级处于半充满状态.
X、Y、Z、Q、R为原子序数依次增大的前四周期元素.X的一种1﹕2型氢化物分子中既有σ键又有π键,且分子中所有原子共平面;Z的L层有2个未成对电子;Q是所在周期中电负性最大的元素,QZ2可替代Q2作新的自来水消毒剂;R在周期表中位于d区,其基态原子有两个能级处于半充满状态.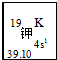 我国的四大发明之一黑火药,爆炸时反应的化学方程式为:S+2KNO3+3C→K2S+3CO2↑+N2↑.请根据其中所含的元素回答下列问题:
我国的四大发明之一黑火药,爆炸时反应的化学方程式为:S+2KNO3+3C→K2S+3CO2↑+N2↑.请根据其中所含的元素回答下列问题: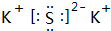 .
.
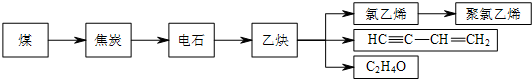
 ,随意丢弃聚氯乙烯制品会造成白色污染.
,随意丢弃聚氯乙烯制品会造成白色污染.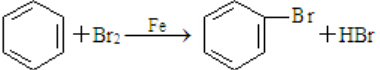 ,该反应中反应物溴应该选用液溴(填“溴水”或“液溴”).
,该反应中反应物溴应该选用液溴(填“溴水”或“液溴”).