题目内容
现用氯水来制取含有次氯酸的溶液,既要提高溶液中HClO物质的量浓度,又要降低溶液中HCl浓度,下列措施可以采用的是( )
| A、加热挥发HCl |
| B、加水使平衡向正反应方向移动 |
| C、加NaOH固体 |
| D、加CaCO3 固体 |
考点:弱电解质在水溶液中的电离平衡
专题:
分析:反应Cl2+H2O?HCl+HClO达到平衡后,要使HClO浓度增加,又要降低溶液中HCl浓度,应使平衡向正反应方向移动,HCl为强酸,HClO为弱酸,酸性比碳酸弱,以此解答该题.
解答:
解:A.加热,降低氯气的溶解度,平衡逆向移动,能使HClO、HCl浓度均减小,故A错误;
B.加水使平衡向正反应方向移动,但总体积增大,则HClO浓度减小,故B错误;
C、加入NaOH,与HCl、HClO均反应,平衡向正反应方向移动,HClO浓度减小,故C错误;
D、加CaCO3固体,与HCl反应,而与HClO不反应,平衡正向移动,HClO浓度增加,又降低溶液中HCl浓度,故D正确;
故选D.
B.加水使平衡向正反应方向移动,但总体积增大,则HClO浓度减小,故B错误;
C、加入NaOH,与HCl、HClO均反应,平衡向正反应方向移动,HClO浓度减小,故C错误;
D、加CaCO3固体,与HCl反应,而与HClO不反应,平衡正向移动,HClO浓度增加,又降低溶液中HCl浓度,故D正确;
故选D.
点评:本题考查化学平衡的影响,题目难度不大,本题易错点为D,注意加入水,溶液体积增大的倍数要大于HClO物质的量增大的倍数,HClO浓度降低.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
下列说法正确的是( )
| A、通常情况下,植物油的熔点比动物油的熔点高 |
| B、人体中,油脂主要在胃中被消化吸收 |
| C、质量相同的油脂和葡萄糖完全氧化时,油脂产生的能量比葡萄糖的高 |
| D、油脂在人体中,能够被氧化放出能量的主要是油脂水解生成的甘油 |
已知:金属铁(含杂质碳)在酸性溶液中发生析氢腐蚀,总反应方程式为:Fe+2H+═Fe2++H2↑;铁在中性或碱性溶液中发生吸氧腐蚀,总反应式为:4Fe+3O2+6H2O═4Fe(OH)3↓.某课外活动小组,将剪下的一块铁片放入锥形瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞试液,按图装置进行实验,数分钟后观察,下列现象不可能出现的是( )
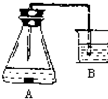

| A、铁被腐蚀 |
| B、B中导气管里形成一段水柱 |
| C、金属片剪口处变红 |
| D、B中导气管中产生气泡 |
下列方程式属于水解反应的是( )
| A、HCO3-+H2O?H3O++CO32- |
| B、H2O+H2O?H3O++H+ |
| C、HCO3-+OH-=H2O+CO32- |
| D、CO32-+H2O?HCO3-+OH- |
下列说法正确的是( )
| A、6.02×1023个碳原子就是阿伏加德罗常数 |
| B、1mol氧就是6.02×1023个氧分子. |
| C、1molNa失去1mol电子生成1molNa+ |
| D、摩尔是七个基本物理量之一 |

