题目内容
8.某学习小组研究“不同条件对化学反应速率影响的研究”,选用4mL0.01mol•L-1KMnO4溶液与2mL0.1mol•L-1H2C2O4溶液在稀硫酸中进行实验,改变条件如表:(1)如果研究催化剂对化学反应速率的影响,使用实验①和②(用①-④表示,下同);如果研究温度对化学反应速率的影响,使用实验①和③.
(2)对比实验①和④,可以研究草酸的浓度或反应物的浓度对化学反应速率的影响,实验④中加入1mL蒸馏水的目的是确保①和④组对比实验中c(KMnO4)不变,或确保溶液总体积不变.
| 组别 | 草酸的体积/mL | 温度/℃ | 其它物质 |
| ① | 2mL | 20 | |
| ② | 2mL | 20 | 2滴饱和MnSO4溶液 |
| ③ | 2mL | 30 | |
| ④ | 1mL | 20 | 1mL蒸馏水 |
分析 (1)研究催化剂对化学反应速率的影响,应保证温度、浓度相同;研究温度对化学反应速率的影响,应保证浓度、不使用催化剂相同;
(2)实验①④硫酸的浓度不同,少量蒸馏水,溶液的体积相同.
解答 解:(1)研究催化剂对化学反应速率的影响,应保证温度、浓度相同,则选实验①②;研究温度对化学反应速率的影响,应保证浓度、不使用催化剂相同,则选实验①③,故答案为:①、②;①、③;
(2)实验①④硫酸的浓度不同,可研究浓度对反应速率的影响,加少量蒸馏水确保两实验中总体积相等,可使①④中硫酸浓度不同,
故答案为:草酸的浓度或反应物的浓度;确保①和④组对比实验中c(KMnO4)不变,或确保溶液总体积不变.
点评 本题考查氧化还原反应及影响反应速率的因素,注意控制变量法研究影响因素,把握表格中的数据分析及应用,题目难度不大.

练习册系列答案
相关题目
18.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在反应KC1O3+6HCl(浓)═KC1+3C12↑+3H2O中,每生成3 mol Cl2转移的电子数为NA | |
| B. | 1 mol K2S固体中含有3 NA个离子 | |
| C. | 1 mol 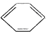 分子中含碳碳双键数为3 NA 分子中含碳碳双键数为3 NA | |
| D. | 含有NA个氖原子的氖气在标准状况下的体积约为11.2 L |
19.在一定温度下,将一包白色无水硫酸铜粉末投入到150g蒸馏水中,充分搅拌过滤得到一定质量的蓝色晶体和84g滤液.又知此温度下无水硫酸铜的溶解度为40g,则此包无水硫酸铜的质量是( )
| A. | 60 g | B. | 66 g | C. | 90 g | D. | 184 g |
16.某化学兴趣小组进行了有关Cu、硝酸、硫酸化学性质的实验,实验过程如图所示.下列有关说法正确的是( )


| A. | 实验①中溶液呈蓝色,试管口有红棕色气体产生,说明稀硝酸被Cu还原为NO2 | |
| B. | 实验③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸强 | |
| C. | 实验③发生反应的化学方程式为:3Cu+Cu(NO3)2+4H2SO4═4CuSO4+2NO↑+4H2O | |
| D. | 由上述实验可得出结论:Cu在常温下既可以和稀硝酸反应,也可以和稀硫酸反应 |
3.溶液、胶体和浊液这三种分散系的本质区别是( )
| A. | 是否是大量分子或离子的集合体 | B. | 分散质微粒直径的大小不同 | ||
| C. | 是否有丁达尔效应 | D. | 是否均一、稳定、透明 |
13. (1)已知:N2(g)+O2(g)═2NO(g)△H1=+180.5kJ/mol
(1)已知:N2(g)+O2(g)═2NO(g)△H1=+180.5kJ/mol
N2(g)+3H2(g)?2NH3(g)△H2=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H3=-483.6kJ/mol
写出氨气催化氧化生成一氧化氮气体和水蒸气的热化学方程式4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-905.0kJ/mol.
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)?2NH3(g)反应的影响.实验结果如图所示:(图中T表示温度,n表示物质的量)
①图象中T2和T1的关系是:T2低于T1(填“高于”“低于”“等于”“无法确定”)
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是c(填字母).
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注:一定温度下可发生下列反应:2N2O5(g)→4NO2(g)+O2(g)△H>0下表为反应在T1温度下的部分实验数据
①500s内NO2的平均生成速率为0.00592mol•L-1•s-1.
②该反应的化学平衡常数表达式为K=$\frac{{c}^{4}(N{O}_{2})•c({O}_{2})}{{c}^{2}({N}_{2}{O}_{5})}$.
 (1)已知:N2(g)+O2(g)═2NO(g)△H1=+180.5kJ/mol
(1)已知:N2(g)+O2(g)═2NO(g)△H1=+180.5kJ/molN2(g)+3H2(g)?2NH3(g)△H2=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H3=-483.6kJ/mol
写出氨气催化氧化生成一氧化氮气体和水蒸气的热化学方程式4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-905.0kJ/mol.
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)?2NH3(g)反应的影响.实验结果如图所示:(图中T表示温度,n表示物质的量)
①图象中T2和T1的关系是:T2低于T1(填“高于”“低于”“等于”“无法确定”)
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是c(填字母).
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注:一定温度下可发生下列反应:2N2O5(g)→4NO2(g)+O2(g)△H>0下表为反应在T1温度下的部分实验数据
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
②该反应的化学平衡常数表达式为K=$\frac{{c}^{4}(N{O}_{2})•c({O}_{2})}{{c}^{2}({N}_{2}{O}_{5})}$.
19.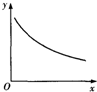 在某密闭容器中充入H2S和O2,发生反应:2H2S(g)+O2(g)?S2(g)+2H2O(g)△H<0,达到平衡后,若仅改变横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势符合图象的是( )
在某密闭容器中充入H2S和O2,发生反应:2H2S(g)+O2(g)?S2(g)+2H2O(g)△H<0,达到平衡后,若仅改变横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势符合图象的是( )
 在某密闭容器中充入H2S和O2,发生反应:2H2S(g)+O2(g)?S2(g)+2H2O(g)△H<0,达到平衡后,若仅改变横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势符合图象的是( )
在某密闭容器中充入H2S和O2,发生反应:2H2S(g)+O2(g)?S2(g)+2H2O(g)△H<0,达到平衡后,若仅改变横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势符合图象的是( )| 选项 | x | y |
| A | 温度 | 混合气体平均相对分子质量 |
| B | 压强 | S2气体体积分数 |
| C | 容器体积 | H2S浓度 |
| D | O2浓度 | 平衡常数 |
| A. | A | B. | B | C. | C | D. | D |
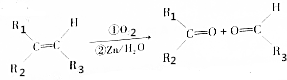
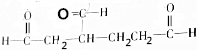 和
和 各1mol.
各1mol.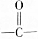 ),产物与烃分子中原子个数相等的元素有C、H.
),产物与烃分子中原子个数相等的元素有C、H. 可简写为
可简写为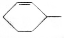 ,其中线表示化学键,线的端点、折点或交点表示碳原子,碳原子剩余的化合价用氢原子补足.写出A所有可能的结构简式:
,其中线表示化学键,线的端点、折点或交点表示碳原子,碳原子剩余的化合价用氢原子补足.写出A所有可能的结构简式: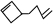 、
、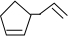 、
、 .
.