题目内容
下列判断中,正确的是( )
| A、30%和H2O2溶液中加入MnO2可制得O2,MnO2做氧化剂 |
| B、SO2和CO2都属于酸性氧化物,Na2O和Al2O3都属于碱性氧化物 |
| C、在NH4Cl水溶液中,既存在水解平衡,又存在电离平衡 |
| D、O2在放电条件下生成O3属于化学变化,煤干馏得到焦炭属于物理变化 |
考点:氧化还原反应,物理变化与化学变化的区别与联系,酸、碱、盐、氧化物的概念及其相互联系,盐类水解的原理
专题:物质的分类专题,氧化还原反应专题,盐类的水解专题
分析:A.二氧化锰作催化剂;
B.和碱反应只生成盐和水的氧化物是酸性氧化物,和酸反应只生成盐和水的氧化物是碱性氧化物;
C.氯化铵是强酸弱碱盐,易水解,水是弱电解质,弱电解质在水溶液里存在电离平衡;
D.原子核不变的情况下,有新物质生成的变化是化学变化,没有新物质生成的变化是物理变化.
B.和碱反应只生成盐和水的氧化物是酸性氧化物,和酸反应只生成盐和水的氧化物是碱性氧化物;
C.氯化铵是强酸弱碱盐,易水解,水是弱电解质,弱电解质在水溶液里存在电离平衡;
D.原子核不变的情况下,有新物质生成的变化是化学变化,没有新物质生成的变化是物理变化.
解答:
解:A.该反应中氧化剂和还原剂都是双氧水,二氧化锰作催化剂,只改变化学反应速率,故A错误;
B.氧化铝是两性氧化物,故B错误;
C.氯化铵易水解,氯化铵溶液中的水是弱电解质,所以在氯化铵溶液中存在水解平衡和电离平衡,故C正确;
D.煤的干馏有新物质生成,所以属于化学变化,故D错误;
故选C.
B.氧化铝是两性氧化物,故B错误;
C.氯化铵易水解,氯化铵溶液中的水是弱电解质,所以在氯化铵溶液中存在水解平衡和电离平衡,故C正确;
D.煤的干馏有新物质生成,所以属于化学变化,故D错误;
故选C.
点评:本题以氧化还原反应为载体考查的知识点较综合,易错选项是C,注意氯化铵溶液中,虽然氯化铵的电离不存在电离平衡,但水的电离存在电离平衡,为易错点.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
钛(Ti)被称为“生物金属”,由Ti0Ρ制取Ti的主要反应:
①Ti02+2Cl2+2C
TiCl4+2CO
②TICl4+2Mg
2MgCl2+Ti
下列说法不正确的是( )
①Ti02+2Cl2+2C
| ||
②TICl4+2Mg
| ||
下列说法不正确的是( )
| A、反应①②都是氧化还原反应 |
| B、反应②是置换反应 |
| C、反应①中Ti02:是氧化剂 |
| D、反应②中每生成1mol Ti转移4 mol电子 |
下列说法正确的是( )
| A、将浓度为0.1mol?L-1 HF溶液加水不断稀释过程中,c( H+) 和c ( OH-)都会减小 |
| B、为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的PH.若PH>7,则H2A是弱酸;若PH<7,则H2A是强酸 |
| C、将SO2通入一定量KOH溶液,所得溶液呈中性,该溶液中一定含KHSO3 |
| D、用0.200mol?L-1 NaOH标准溶液滴定浓度均为0.1mol?L-1 的HCl与CH3COOH的混合液,至中性时,溶液中的酸恰好被完全中和 |
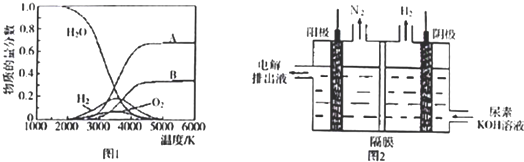
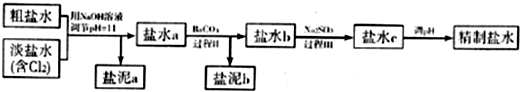

 在汽车上安装催化转化器可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)相互反应生成无毒害物质,减少汽车尾气污染.
在汽车上安装催化转化器可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)相互反应生成无毒害物质,减少汽车尾气污染.

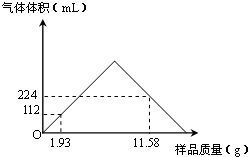 含钡化合物在实验室和工业生产中都有广泛的用途.
含钡化合物在实验室和工业生产中都有广泛的用途.