题目内容
利用下表中图示实验装置,不能得出相应实验结论的是( )
| ① | ② | ③ | 实验结论 | 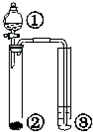 | |
| A | 稀醋酸 | CaCO3 | 澄清石灰水 | 酸性:醋酸>碳酸 | |
| B | 硫酸 | Na2SO3 | 溴水 | SO2具有还原性 | |
| C | 浓盐酸 | KMnO4 | 淀粉KI溶液 | 氧化性:KMnO4>Cl2>I2 | |
| D | 盐酸 | Na2CO3 | Na2SiO3 | 非金属性:Cl>C>Si |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:
分析:A.强酸能和弱酸的盐反应生成弱酸;
B.硫酸和亚硫酸钠反应生成二氧化硫,二氧化硫能被强氧化剂氧化;
C.浓盐酸和高锰酸钾溶液反应生成氯气,氯气能置换出碘单质,碘遇淀粉试液变蓝色,自发进行的同一氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强.
B.硫酸和亚硫酸钠反应生成二氧化硫,二氧化硫能被强氧化剂氧化;
C.浓盐酸和高锰酸钾溶液反应生成氯气,氯气能置换出碘单质,碘遇淀粉试液变蓝色,自发进行的同一氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强.
解答:
解:A.强酸能和弱酸的盐反应生成弱酸,稀醋酸和碳酸钙反应生成二氧化碳,二氧化碳能使澄清石灰水变浑浊,只要石灰水变浑浊就能证明酸性:醋酸>碳酸,故A正确;
B.硫酸和亚硫酸钠反应生成二氧化硫,二氧化硫能被强氧化剂氧化,溴具有强氧化性,只要溴水褪色,就说明二氧化硫具有还原性,故B正确;
C.浓盐酸和高锰酸钾溶液反应生成氯气,氯气能置换出碘单质,碘遇淀粉试液变蓝色,自发进行的同一氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,只要淀粉碘化钾试纸变蓝色,就说明发生这一系列的反应,第一个反应中高锰酸钾作氧化剂、氯气是氧化产物,第二个反应中氯气是氧化剂、碘是氧化产物,所以氧化性:KMnO4>Cl2>I2,故C正确;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强,盐酸和碳酸钠反应生成二氧化碳,二氧化碳和硅酸钠溶液反应生成硅酸,能证明酸性盐酸>碳酸>硅酸,HCl不是Cl元素的最高价氧化物的水化物,所以不能证明非金属性Cl>C>Si,故D错误;
故选D.
B.硫酸和亚硫酸钠反应生成二氧化硫,二氧化硫能被强氧化剂氧化,溴具有强氧化性,只要溴水褪色,就说明二氧化硫具有还原性,故B正确;
C.浓盐酸和高锰酸钾溶液反应生成氯气,氯气能置换出碘单质,碘遇淀粉试液变蓝色,自发进行的同一氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,只要淀粉碘化钾试纸变蓝色,就说明发生这一系列的反应,第一个反应中高锰酸钾作氧化剂、氯气是氧化产物,第二个反应中氯气是氧化剂、碘是氧化产物,所以氧化性:KMnO4>Cl2>I2,故C正确;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强,盐酸和碳酸钠反应生成二氧化碳,二氧化碳和硅酸钠溶液反应生成硅酸,能证明酸性盐酸>碳酸>硅酸,HCl不是Cl元素的最高价氧化物的水化物,所以不能证明非金属性Cl>C>Si,故D错误;
故选D.
点评:本题考查化学实验方案评价,侧重考查实验操作、分析能力,明确实验原理是解本题关键,易错选项是D,注意D中能实现的实验目的、不能实现的实验目的,为易错点.

练习册系列答案
相关题目
氮氧化物与悬浮在大气中海盐粒子的相互反应:4NO2(g)+2NaCl(s)═2NaNO3(s)+2NO(g)+Cl2(g),△H在恒温条件下,向2L恒容密闭容器中加入0.4mol NO2和0.2mol NaCl,10min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为α.下列叙述中正确的是( )
| A、10min内NO浓度变化表示的速率v(NO)=0.01 mol?L-1?min-1 |
| B、若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于α |
| C、若升高温度,平衡逆向移动,则该反应的△H>0 |
| D、若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),则反应将向逆反应方向进行 |
理论上不能用于设计成原电池的反应是( )
| A、2H2(g)+O2(g)═2H2O(l)△H<0 |
| B、HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H<0 |
| C、2Al(s)+3Cl2(g)═2AlCl3(s)△H<0 |
| D、Zn(s)+2HCl(aq)═ZnCl2+H2(g)△H<0 |
下列各组离子中,能在溶液中大量共存的是( )
| A、H+、Ca2+、Cl-、AlO2- |
| B、K+、H+、NO3-、Cl- |
| C、Na+、Fe3+、I-、SO42- |
| D、Na+、Ca2+、Cl-、SO42- |
下列表述正确的是( )
| A、常温下pH=1的一元酸和pH=13的一元碱等体积混合所得溶液一定呈中性 |
| B、常温下,pH=7的氨水与氯化铵的混合溶液中,Cl-与NH4+的浓度关系c(Cl-)>c(NH4+) |
| C、10mL 0.10mol?L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是C(Na+)>C(CH3COO-)>C(OH-)>C(H+) |
| D、中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同 |
下列除去杂质的方法正确的是( )
| 物质 | 杂质 | 试剂 | 主要操作 | |
| A | NaHCO3固体 | Na2CO3固体 | / | 加热 |
| B | Al2O3 | Fe2O3 | 盐酸 | 过滤 |
| C | KBr溶液 | Br2 | KOH溶液 | 分液 |
| D | Cl2 | HCl | 饱和食盐水 | 洗气 |
| A、A | B、B | C、C | D、D |
有机物A的分子式为C8H16O2,在酸性条件下A能水解为甲和乙两种有机物,甲在一定的条件下可以催化氧化得到乙,则A的可能结构有( )
| A、2种 | B、4种 | C、6种 | D、8种 |
