题目内容
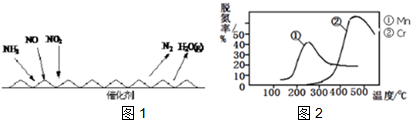
氮氧化物与悬浮在大气中海盐粒子的相互反应:4NO2(g)+2NaCl(s)═2NaNO3(s)+2NO(g)+Cl2(g),△H在恒温条件下,向2L恒容密闭容器中加入0.4mol NO2和0.2mol NaCl,10min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为α.下列叙述中正确的是( )
| A、10min内NO浓度变化表示的速率v(NO)=0.01 mol?L-1?min-1 |
| B、若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于α |
| C、若升高温度,平衡逆向移动,则该反应的△H>0 |
| D、若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),则反应将向逆反应方向进行 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、根据三行式结合公式v(NO)=
,来分析解答;
B、正反应是气体体积缩小的反应,若保持其他条件不变,在恒压下进行该反应,气体体积缩小,相当于体积不变,增大压强;
C、根据平衡移动的原理分析解答;
D、根据平衡常数与浓度商的大小来分析判断.
| △c |
| △t |
B、正反应是气体体积缩小的反应,若保持其他条件不变,在恒压下进行该反应,气体体积缩小,相当于体积不变,增大压强;
C、根据平衡移动的原理分析解答;
D、根据平衡常数与浓度商的大小来分析判断.
解答:
解:在恒温条件下,向2L恒容密闭容器中加入0.4mol NO2和0.2mol NaCl,10min反应达到平衡时n(NaNO3)=0.1mol,依据平衡三段式列式计算;
4NO2(g)+2NaCl(s)═2NaNO3(s)+2NO(g)+Cl2(g),
起始量(mol) 0.4 0.2 0 0 0
变化量(mol) 0.2 0.1 0.1 0.1 0.05
平衡量(mol) 0.2 0.1 0.1 0.1 0.05
所以K=
=0.625,
A、根据公式v(NO)=
=
=0.005mol?L-1?min-1,故A错误;
B、正反应是气体体积缩小的反应,若保持其他条件不变,在恒压下进行该反应,气体体积缩小,相当于体积不变,增大压强,平衡向气体体积减小的方向移动,所以NO2的转化率变大,故B正确;
C、若升高温度,平衡逆向移动,逆反应是吸热反应,正反应是放热反应,所以该反应的△H<0,故C错误;
D、Qc=
=80>K,所以平衡逆向移动,故D正确;
故选:BD.
4NO2(g)+2NaCl(s)═2NaNO3(s)+2NO(g)+Cl2(g),
起始量(mol) 0.4 0.2 0 0 0
变化量(mol) 0.2 0.1 0.1 0.1 0.05
平衡量(mol) 0.2 0.1 0.1 0.1 0.05
所以K=
(
| ||||
(
|
A、根据公式v(NO)=
| △c |
| △t |
| ||
| 10 |
B、正反应是气体体积缩小的反应,若保持其他条件不变,在恒压下进行该反应,气体体积缩小,相当于体积不变,增大压强,平衡向气体体积减小的方向移动,所以NO2的转化率变大,故B正确;
C、若升高温度,平衡逆向移动,逆反应是吸热反应,正反应是放热反应,所以该反应的△H<0,故C错误;
D、Qc=
(
| ||||
(
|
故选:BD.
点评:本题考查了化学平衡常数和化学反应速率的计算,影响化学平衡移动的因素分析应用,学生要学会应用平衡常数来判断反应进行的方向,掌握基础是关键,题目难度中等.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
下列离子方程式正确的是( )
| A、铜片加入稀硝酸中:3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O |
| B、向小苏打溶液中加入醋酸:HCO3-+H+═CO2↑+H2O |
| C、向HI溶液中加入Fe(OH)3固体:Fe(OH)3+3H═Fe3++3H2O |
| D、向MgSO4溶液中加入Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ |
在某一透明溶液中加入Al片有H2生成,则此溶液中一定可大量存在的离子组是( )
| A、AlO2-,K+,SO42-,Cl- |
| B、K+,Br-,SO42-,Na+ |
| C、Fe3+,NO3-,Na+,S2- |
| D、I-,Cl-,Mg2+,SO42- |
下列有关原子结构和元素周期律表述正确的是( )
| A、原子序数为15的元素的最高化合价为+3 |
| B、第ⅦA族元素是同周期中非金属性最强的元素 |
| C、Li、Na、K、Rb、Cs的得电子能力逐渐增强 |
| D、原子序数为12的元素位于元素周期表的第三周期的ⅡA族 |
下列有关物质存放的说法,正确的是( )
| A、金属钠保存在无水乙醇中 |
| B、冷的浓H2SO4存放于敞口铝制容器中 |
| C、少量的白磷保存在二硫化碳中 |
| D、氯气液化后贮存于钢瓶中 |