题目内容
7.下列有关NaAlO2和Na2S混合溶液的叙述正确的是( )| A. | 该溶液中,H+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,Al3+、K+、NO3-可以大量共存 | |
| C. | 向该溶液中滴入少量FeCl3溶液,可能会发生:2Fe3++S2-=2Fe2++S↓ | |
| D. | 向该溶液中同时加入过量的盐酸和过量的Na2SO3溶液,每产生1mol的硫沉淀,转移电子数约为1.024×1024个 |
分析 A.离子之间结合生成沉淀或弱电解质;
B.离子之间相互促进水解;
C.滴入少量FeCl3溶液,与硫离子发生氧化还原反应;
D.加入过量的盐酸和过量的Na2SO3溶液,发生6H++SO32-+2S2-=3S↓+3H2O.
解答 解:A.H+分别与AlO2-、S2-结合生成沉淀或弱电解质,不能共存,故A错误;
B.Al3+分别与AlO2-、S2-相互促进水解,不能共存,故B错误;
C.滴入少量FeCl3溶液,与硫离子发生氧化还原反应,离子反应为2Fe3++S2-=2Fe2++S↓,故C正确;
D.加入过量的盐酸和过量的Na2SO3溶液,发生6H++SO32-+2S2-=3S↓+3H2O,则每产生1mol的硫沉淀,转移电子数约为$\frac{4}{3}$×6.02×1023个,故D错误;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重水解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.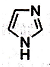 离子液体在有机合成、无机合成等方面有着重要应用.咪唑是合成“离子液体”的一种原料,其结构如图所示.下列有关咪唑说法不正确的是( )
离子液体在有机合成、无机合成等方面有着重要应用.咪唑是合成“离子液体”的一种原料,其结构如图所示.下列有关咪唑说法不正确的是( )
 离子液体在有机合成、无机合成等方面有着重要应用.咪唑是合成“离子液体”的一种原料,其结构如图所示.下列有关咪唑说法不正确的是( )
离子液体在有机合成、无机合成等方面有着重要应用.咪唑是合成“离子液体”的一种原料,其结构如图所示.下列有关咪唑说法不正确的是( )| A. | 化学式C3H4N2 | |
| B. | 分子中含有一种非极性键和两种极性键 | |
| C. | 可以发生取代、加成、氧化反应 | |
| D. | 一氯取代物的同分异构体共有4种 |
18.用已知浓度的NaOH滴定未知浓度的盐酸,下列操作(其他操作正确)会造成测定结果偏高的是( )
| A. | 滴定终点读数时俯视度数 | |
| B. | 酸式滴定管使用前,水洗后未用待测盐酸润洗 | |
| C. | 锥形瓶洗净后未干燥 | |
| D. | 碱式滴定管滴定前尖嘴部分有气泡,滴定后气泡消失 |
15.下列有机物可以形成顺反异构的是( )
| A. | l-丁烯 | B. | 2-己烯 | ||
| C. | 2-甲基-2-丁烯 | D. | 2,3-二 甲基-2-丁烯 |
2.将一定量的乙二酸(分子式为C2H2O4)完全燃烧后的所有产物,全部通人过量的石灰水中.完全被吸收,经过滤得到40g沉淀,滤液的质量比原石灰水的质量减少了(不考虑过滤时液体质量的损失)( )
| A. | 11.6g | B. | 15.2g | C. | 18.8g | D. | 21.2g |
12.下列对实验现象的解释与结论正确的是( )
| 实验现象 | 解释与结论 | |
| A | 向铜和稀硫酸的混合物中加入无色溶液,溶液逐渐变成蓝色,铜逐渐溶解 | 该无色溶液一定是硝酸 |
| B | 将某气体通入品红溶液中,品红溶液颜色 | 该气体一定是SO2 |
| C | SO2气体通过Ba(NO3)2溶液中,溶液出现浑浊现象 | 说明有BaSO3沉淀生成 |
| D | 向NaHCO3溶液中滴加酚酞试液,加热时溶液由淡红色变为红色,冷却后溶液由红色变为淡红色 | 说明HCO3在水溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
19.2015年底,我市出现重度雾霾天气PM2.5爆表,PM2.5是高密度人口经济及社会活动必然排放的大量细颗粒物,微粒直径在2.5微米以下,下列微粒直径与2.5微米最接近的是( )
| A. | 原子核 | B. | 原子 | ||
| C. | 胶体粒子 | D. | 悬浊液的分散质粒子 |
16.下列有机化合物命名正确的是( )
| A. | 2-甲基-3-乙基-戊烷 | B. | 3、4-二甲基戊烷 | ||
| C. | 2-乙基丁烷 | D. | 1-甲基丙烷 |