题目内容
一定能在下列溶液中大量共存的离子组是( )
| A、能使pH试纸变深蓝色的溶液中,Na+、AlO2-、S2-、CO32- |
| B、由水电离产生的c(H+)=1×10-12mol/L的溶液中:NH4+、Na+、Cl-、HCO3- |
| C、含有大量Fe3+的溶液,SCN-、I-、K+、Br- |
| D、澄清透明的无色溶液中:ClO-、MnO4-、Al3+、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:A.能使pH试纸变深蓝色的溶液,显碱性;
B.由水电离产生的c(H+)=1×10-12mol/L的溶液,为酸或碱溶液;
C.离子之间结合生成络离子,离子之间发生氧化还原反应;
D.MnO4-为紫色.
B.由水电离产生的c(H+)=1×10-12mol/L的溶液,为酸或碱溶液;
C.离子之间结合生成络离子,离子之间发生氧化还原反应;
D.MnO4-为紫色.
解答:
解:A.能使pH试纸变深蓝色的溶液,显碱性,该组离子之间不反应,可大量共存,故A正确;
B.由水电离产生的c(H+)=1×10-12mol/L的溶液,为酸或碱溶液,碱性溶液中不能大量存在NH4+、HCO3-,酸性溶液中不能存在HCO3-,故B错误;
C.Fe3+、SCN-结合生成络离子,Fe3+、I-发生氧化还原反应,不能大量共存,故C错误;
D.MnO4-为紫色,与无色溶液不符,故D错误;
故选A.
B.由水电离产生的c(H+)=1×10-12mol/L的溶液,为酸或碱溶液,碱性溶液中不能大量存在NH4+、HCO3-,酸性溶液中不能存在HCO3-,故B错误;
C.Fe3+、SCN-结合生成络离子,Fe3+、I-发生氧化还原反应,不能大量共存,故C错误;
D.MnO4-为紫色,与无色溶液不符,故D错误;
故选A.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应及氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
下列有机物的名称正确的是( )
| A、3-氯丙烷 |
| B、2-甲基-2-乙基丁烷 |
| C、3-丁烯 |
| D、2,3-二甲基戊烷 |
NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、实验室以H2O2和MnO2为原料制取O2,每生成1mol O2转移2NA个电子 |
| B、标准状况下,0.5NA个H2O分子所占有的体积为11.2L |
| C、1mol 硫酸钾中阴离子所带电荷数为NA |
| D、18.0g NH4+中所含的质子数为10NA |
在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为手性碳原子,凡是有一个手性碳原子的物质一定具有光学活性.例如,有机化合物 有光学活性,分别发生下列反应:①与甲酸发生酯化反应②与氢氧化钠水溶液共热③与银氨溶液作用④在催化剂存在下与氢气作用.生成的有机物中无光学活性的是( )
有光学活性,分别发生下列反应:①与甲酸发生酯化反应②与氢氧化钠水溶液共热③与银氨溶液作用④在催化剂存在下与氢气作用.生成的有机物中无光学活性的是( )
 有光学活性,分别发生下列反应:①与甲酸发生酯化反应②与氢氧化钠水溶液共热③与银氨溶液作用④在催化剂存在下与氢气作用.生成的有机物中无光学活性的是( )
有光学活性,分别发生下列反应:①与甲酸发生酯化反应②与氢氧化钠水溶液共热③与银氨溶液作用④在催化剂存在下与氢气作用.生成的有机物中无光学活性的是( )| A、①②④ | B、②③④ |
| C、①②③ | D、①③④ |
下列关于有机物的说法正确的是( )
| A、乙醇、乙烷和乙酸都可以与钠反应生成氢气 |
| B、乙醇可以被酸性重铬酸钾溶液直接氧化为乙酸 |
| C、乙烯使溴水和酸性高锰酸钾溶液褪色的反应均属于加成反应 |
| D、汽油、柴油和植物油都是碳氢化合物 |
一定量Fe和Fe2O3的混合物投入250ml 2mol/L的硝酸中,反应共生成1.12L NO(标准状况下),再向反应后的溶液中加入1mol/L的硝酸NaOH溶液,当沉淀完全时所加NaOH溶液的体积最少是( )
| A、450mL | B、500mL |
| C、400mL | D、不能确定 |
根据下列信息判断氢气燃烧生成水时的热量变化,其中一定正确的是( )
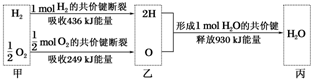

| A、H2O分解为H2与O2时放出热量 |
| B、生成1mol H2O时吸收热量245kJ |
| C、氢气和氧气的总能量小于水的能量 |
| D、甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙 |
向一定量的盐酸中逐滴加入NaAlO2溶液,生成沉淀Al(OH)3的量随NaAlO2加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )

A、a点对应的溶液中:NH
| ||||||
B、b点对应的溶液中:Na+、S2-、SO
| ||||||
C、c点对应的溶液中:Ag+、Ba2+、K+、NO
| ||||||
D、d点对应的溶液中:K+、S2-、I-、CO
|