题目内容
 在量热计中(如图)将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.
在量热计中(如图)将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.(1)试求CH3COOH的中和热△H
(2)CH3COOH的中和热的文献值为56.1kJ?mol-1,你认为(1)中测得的实验值有偏差可能的原因是
(3)实验中NaOH过量的目的是
(4)你认为CH3COOH的中和热与HCl的中和热数值相比,
考点:反应热和焓变
专题:化学反应中的能量变化
分析:(1)根据化学反应热的计算公式Q=-cm△T来计算;
(2)根据中和热的测定中能够导致放出的热量偏低的因素进行解答;
(3)酸和碱反应测中和热时,为了保证一方全部反应,往往需要另一试剂稍稍过量,减少实验误差;
(4)醋酸是弱酸,电离过程需要吸收能量.
(2)根据中和热的测定中能够导致放出的热量偏低的因素进行解答;
(3)酸和碱反应测中和热时,为了保证一方全部反应,往往需要另一试剂稍稍过量,减少实验误差;
(4)醋酸是弱酸,电离过程需要吸收能量.
解答:
解:(1)CH3COOH的中和热Q=△H=Q=-cm△T=
=-5.33×104 J?mol-1=-53.3 kJ?mol-1,
故答案为:-53.3 kJ?mol-1;
(2)CH3COOH的中和热的文献值为-56.1kJ/mol,实际上测定数值偏低,可能原因有:①量热计的保温瓶效果不好,②酸碱溶液混合不迅速,③温度计不够精确等,
故答案为:①量热计的保温瓶绝热效果不好、②酸碱溶液混合不迅速、③温度计不够精确等;
(3)酸和碱反应测中和热时,为了保证一方全部反应,往往需要另一试剂稍稍过量,减少实验误差,
故答案为:过量的碱能保证CH3COOH完全被中和,从而提高实验准确度;
(4)醋酸是弱酸,电离过程需要吸收能量,所以CH3COOH的中和热与HCl的中和热数值相比,HCl较大,
故答案为:HCl;CH3COOH是弱酸,只是少部分电离,CH3COOH发生电离时要吸热,中和时放热较少.
| [150.5J/K+4.184J?(g?K)-1×200g]×(300.7-298)K |
| 0.05mol |
故答案为:-53.3 kJ?mol-1;
(2)CH3COOH的中和热的文献值为-56.1kJ/mol,实际上测定数值偏低,可能原因有:①量热计的保温瓶效果不好,②酸碱溶液混合不迅速,③温度计不够精确等,
故答案为:①量热计的保温瓶绝热效果不好、②酸碱溶液混合不迅速、③温度计不够精确等;
(3)酸和碱反应测中和热时,为了保证一方全部反应,往往需要另一试剂稍稍过量,减少实验误差,
故答案为:过量的碱能保证CH3COOH完全被中和,从而提高实验准确度;
(4)醋酸是弱酸,电离过程需要吸收能量,所以CH3COOH的中和热与HCl的中和热数值相比,HCl较大,
故答案为:HCl;CH3COOH是弱酸,只是少部分电离,CH3COOH发生电离时要吸热,中和时放热较少.
点评:本题考查中和热的测定,注意掌握测定中和热的原理、操作方法,以及热量计算公式的应用,题目难度中等.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
用惰性电极电解硫酸铜和盐酸的混合溶液,则阴、阳两极产生的气体成分及体积比不可能是( )
| A、阳极为纯净气体,阴、阳两极产生的气体体积比≤1:1 |
| B、阳极为纯净气体,阴、阳两极产生的气体体积比≥1:1 |
| C、阳极为混合气体,阴、阳两极产生的气体体积比≤1:1 |
| D、阳极为混合气体,阴、阳两极产生的气体体积比≥1:1 |
设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A、0.1molN2与0.3molH2在密闭容器催化剂作用下充分反应,生成氨分子数为0.2NA |
| B、标准状况下,11.2L甲醛气体中电子数为8NA |
| C、常温常压下,7.8g苯中含有单键的数目为0.9NA |
| D、1L浓度为1mol?L-1的Na2CO3溶液中含有NA个CO32- |
2014年度诺贝尔化学奖授予了研制出超高分辨率荧光显微镜的三位科学家.该仪器可 用于研究细胞结构和功能等.则下列有关仪器分析说法中错误的是( )
| A、原子吸收光谱仪可用于测定物质中的金属元素 |
| B、质谱仪不能用于分析有机化合物的结构 |
| C、红外光谱仪可用于测定有机化合物的官能团 |
| D、氢核磁共振仪能鉴别CH3COOCH2CH3与CH3CH2COOCH3 |
对于可逆反应C(s)+H2O(g)?CO(g)+H2(g),在一定温度下达到平衡时,其平衡常数表达式正确的是( )
A、K=
| ||
B、K=
| ||
C、K=
| ||
D、K=
|
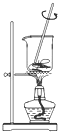
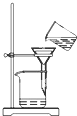
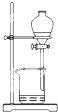
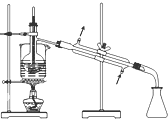
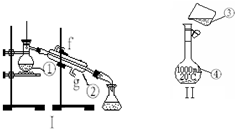 掌握仪器的名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.
掌握仪器的名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.