题目内容
18.相同温度下,下列物质中导电性最强的是( )| A. | 80ml 0.1 mol•L-1NaCl溶液 | B. | 50ml 0.1 mol•L-1MgSO4溶液 | ||
| C. | 100ml 0.1 mol•L-1氨水 | D. | 0.1 mol固体氯化钠 |
分析 溶液的导电性强弱取决于溶液离子浓度大小、离子的电荷,溶液离子浓度越大、电荷越高,导电性越强.
解答 解:A、0.1mol•L-1NaCl溶液中,钠离子和氯离子浓度分别是0.1mol•L-1、0.1mol•L-1;
B、0.1mol•L-1MgSO4溶液中,镁离子和硫酸根离子的浓度分别是0.1mol•L-1、0.1mol•L-1,
C、0.1 mol•L-1氨水中,铵根离子和氢氧根离子的浓度分别为:小于0.1mol•L-1、小于0.1mol•L-1;
D、晶体中离子在静电作用的束缚下不能自由移动,所以不导电;
所以自由移动离子浓度最大、电荷浓度最大的是B,即B中导电性最强.
故选B.
点评 本题考查电解质溶液的导电性,题目难度不大,注意溶液的导电性强弱取决于溶液离子浓度大小和离子的电荷,把握电解质强弱的判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.空气中SO2含量是重要的空气质量指标.
ⅰ、某工厂SO2的排放量规定不得超过0.10mg/(L烟道气),为测定该工厂排放的烟道气中SO2的含量,某同学某次抽取了30.00L烟道气缓慢通过1L水,设SO2完全被吸收,设溶液体积为1L,用1.0×10-3mol/L的饱和碘水(密度为1g/cm3)滴定,反应为SO2+I2+2H2O═H2SO4+2HI,实验所记录数据如下:
(1)取25.00ml的烟道气的水溶液所用仪器名称是酸式滴定管
(2)滴定终点标志为滴入最后一滴试液时,溶液变为蓝色,并半分钟内不褪色
(3)该厂排放的烟道气中SO2的含量为0.512mg/(L烟道气)
ⅱ、该同学在实验室还验证了SO2能否与BaCl2溶液反应的实验.二氧化硫通入氯化钡溶液中理论上不产生沉淀,但当他把SO2通入装有1mol/LBaCl2溶液的试管中后,出现了白色浑浊物.
(1)该白色浑浊物为BaSO4,产生该现象的原因可能是空气和溶液中氧气把H2SO3氧化成了H2SO4,从而生成BaSO4
(2)为了避免产生沉淀,该同学设计了如下实验装置,

请回答下列问题
①反应开始前,先向制取SO2的装置中通入纯净的N2,其作用是:赶出装置中的气体,防止二氧化硫通入氯化钡溶液后的现象受到空气和溶液中氧气的影响.
②该同学认为Ba(NO3)2溶液与BaCl2溶液一样在理论上与SO2也不会反应,请先判断正误错误(填“正确”、“错误”),如不正确则写出SO2与Ba(NO3)2溶液反应的化学方程式Ba(NO3)2+3SO2+2H2O=BaSO4↓+2NO+2H2SO4.
ⅰ、某工厂SO2的排放量规定不得超过0.10mg/(L烟道气),为测定该工厂排放的烟道气中SO2的含量,某同学某次抽取了30.00L烟道气缓慢通过1L水,设SO2完全被吸收,设溶液体积为1L,用1.0×10-3mol/L的饱和碘水(密度为1g/cm3)滴定,反应为SO2+I2+2H2O═H2SO4+2HI,实验所记录数据如下:
| 溶有SO2的溶液体积 | 饱和碘水体积 | 指示剂 | |
| 第一次 | 25.00mL | 6.05 | 2~3滴淀粉 |
| 第二次 | 25.00mL | 7.20 | 2~3滴淀粉 |
| 第三次 | 25.00mL | 5.95 | 2~3滴淀粉 |
(2)滴定终点标志为滴入最后一滴试液时,溶液变为蓝色,并半分钟内不褪色
(3)该厂排放的烟道气中SO2的含量为0.512mg/(L烟道气)
ⅱ、该同学在实验室还验证了SO2能否与BaCl2溶液反应的实验.二氧化硫通入氯化钡溶液中理论上不产生沉淀,但当他把SO2通入装有1mol/LBaCl2溶液的试管中后,出现了白色浑浊物.
(1)该白色浑浊物为BaSO4,产生该现象的原因可能是空气和溶液中氧气把H2SO3氧化成了H2SO4,从而生成BaSO4
(2)为了避免产生沉淀,该同学设计了如下实验装置,

请回答下列问题
①反应开始前,先向制取SO2的装置中通入纯净的N2,其作用是:赶出装置中的气体,防止二氧化硫通入氯化钡溶液后的现象受到空气和溶液中氧气的影响.
②该同学认为Ba(NO3)2溶液与BaCl2溶液一样在理论上与SO2也不会反应,请先判断正误错误(填“正确”、“错误”),如不正确则写出SO2与Ba(NO3)2溶液反应的化学方程式Ba(NO3)2+3SO2+2H2O=BaSO4↓+2NO+2H2SO4.
6.下列说法错误的是( )
| A. | 1H和3H是不同的核素 | |
| B. | 1H、2H、3H、H+和H2是氢元素的五种不同粒子 | |
| C. | 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同 | |
| D. | 石墨和金刚石互为同位素,化学性质相似 |
3.下列有关盐类水解的说法中,正确的是( )
| A. | 所有的盐在水溶液中都能水解 | |
| B. | 盐类水解一定都显酸性或碱性 | |
| C. | 盐类的水解反应是酸碱中和反应的逆反应,因此盐类水解是吸热反应 | |
| D. | 盐类水解抑制了水的电离 |
7.欲分离某CCl4和H2O的混合液,除铁架台、铁圈外,还需要用到的仪器是( )
| A. | 漏斗 | B. | 长颈漏斗 | C. | 分液漏斗 | D. | 直形冷凝管 |
8.如图所示是氨催化氧化制备硝酸的实验装量,下有关叙述正确的是( )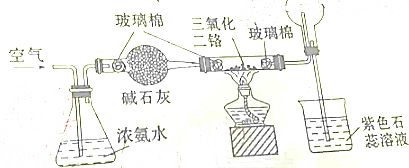

| A. | 烧杯中的紫色石蕊溶液不变色 | |
| B. | 圆底烧瓶中的气体一定为无色 | |
| C. | 加热后,通过三氯化二铬的气体由无色变为红棕色 | |
| D. | 三氯化二铬起氧化剂的作用 |