题目内容
19.下列所述的两者是同种物质的是( )| A. | HCl和盐酸 | B. | 干冰和CO2 | C. | 正丁烷和异丁烷 | D. | 白磷和红磷 |
分析 同种物质具有相同分子式、相同的结构,结合同分异构体、同素异形体、混合物的概念进行解答.
解答 解:A.HCl为化合物,而盐酸为混合物,二者不属于同种物质,故A错误;
B.干冰为固态二氧化碳俗名,则干冰和CO2为同种物质,故B正确;
C.正丁烷和异丁烷的分子式相同、结构不同,二者互为同分异构体,故C错误;
D.白磷和红磷都是磷元素的不同单质,二者互为同素异形体,故D错误;
故选B.
点评 本题考查较为综合,涉及同种物质、同素异形体、同分异构体等知识,题目难度不大,明确五同的概念及判断方法为解答关键,试题侧重 基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
9.下列有关化学用语使用不正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | N2的结构式:N≡N | ||
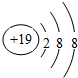
| C. | Na的原子结构示意图: | D. | CH4分子的比例模型: |
7.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | FeCl3溶液中:K+、OH-、SO42-、SCN- | |
| B. | 使酚酞试液变红的溶液中:NH4+、Na+、HCO3-、NO3- | |
| C. | c(OH-)=1mol/L的溶液中:Na+、K+、CO32-、NO3- | |
| D. | c(H+)=1mol/L的溶液中:K+、Na+、Fe2+、NO3- |
14.下列溶液中,能用带磨口玻璃塞的试剂瓶盛放的是( )
| A. | 浓硫酸 | B. | 水玻璃 | C. | 氢氟酸 | D. | 苛性钾溶液 |
4.在锌与某浓度的盐酸反应的实验中,实验员得到下面的结果:
(1)写出实验中发生反应的离子方程式:Zn+2H+=Zn2++H2↑,该反应是放热反应(填“放热”或“吸热”);
(2)仔细观察A~F的实验数据对比,你可以得到关于温度影响反应速率结论,用此结论,计算:55℃时,2g锌薄片溶解于酸中需花12.5 s.
(3)对比结果B与F,解释结果F那么快的原因:B中锌是块状,F中锌是粉末状,粉末状时锌与酸溶液的接触面要比块状时的接触面大得多.
| 锌的质量(g) | 锌的形状 | 温度(℃) | 溶解于酸花的时间(s) | |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | 50 |
| E | 2 | 薄片 | 45 | 25 |
| F | 2 | 粉末 | 15 | 5 |
(2)仔细观察A~F的实验数据对比,你可以得到关于温度影响反应速率结论,用此结论,计算:55℃时,2g锌薄片溶解于酸中需花12.5 s.
(3)对比结果B与F,解释结果F那么快的原因:B中锌是块状,F中锌是粉末状,粉末状时锌与酸溶液的接触面要比块状时的接触面大得多.
11.下列递变规律中,正确的是( )
| A. | Na、Mg、Al、S的还原性依次增强 | |
| B. | O、S、Na、K的原子半径依次增大 | |
| C. | H2S、PH3、HCl、HF的热稳定性依次增强 | |
| D. | Mg(OH)2、Al(OH)3、KOH、Ca(OH)2的碱性依次增强 |
8.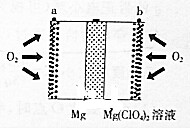 镁空气电池具有比锂电池更好的安全性和更低的成本,主要用于备用电源、军事应用,其工作原理如图所示.下列说法错误的是( )
镁空气电池具有比锂电池更好的安全性和更低的成本,主要用于备用电源、军事应用,其工作原理如图所示.下列说法错误的是( )
 镁空气电池具有比锂电池更好的安全性和更低的成本,主要用于备用电源、军事应用,其工作原理如图所示.下列说法错误的是( )
镁空气电池具有比锂电池更好的安全性和更低的成本,主要用于备用电源、军事应用,其工作原理如图所示.下列说法错误的是( )| A. | 放电时Mg在负极被ClO4-氧化 | |
| B. | 正极的电极反应为:O2+2H2O+4e-═4OH- | |
| C. | 电池总反应为2Mg+O2+2H2O═2Mg(OH)2 | |
| D. | 理论上外电路流过1mol电子时电池总质量增加8.0g |