题目内容
4.在锌与某浓度的盐酸反应的实验中,实验员得到下面的结果:| 锌的质量(g) | 锌的形状 | 温度(℃) | 溶解于酸花的时间(s) | |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | 50 |
| E | 2 | 薄片 | 45 | 25 |
| F | 2 | 粉末 | 15 | 5 |
(2)仔细观察A~F的实验数据对比,你可以得到关于温度影响反应速率结论,用此结论,计算:55℃时,2g锌薄片溶解于酸中需花12.5 s.
(3)对比结果B与F,解释结果F那么快的原因:B中锌是块状,F中锌是粉末状,粉末状时锌与酸溶液的接触面要比块状时的接触面大得多.
分析 (1)锌与盐酸反应生成氯化锌和氢气,中和反应是放热反应;
(2)比较BCD三个实验可以知道,每升高10℃,反应时间缩短为原来的一半;
(3)接触面积越大反应速率越快.
解答 解:(1)锌与盐酸反应离子方程式:Zn+2H+=Zn2++H2↑,中和反应是放热反应,故答案为:Zn+2H+=Zn2++H2↑;放热;
(2)比较BCD三个实验可以知道,每升高10℃,反应时间缩短为原来的一半,55℃时,2g锌薄片溶解于酸中需花12.5s,故答案为:12.5;
(3)接触面积越大反应速率越快,B中锌是块状,F中锌是粉末状,故答案为:B中锌是块状,F中锌是粉末状,粉末状时锌与酸溶液的接触面要 比块状时的接触面大得多.
点评 本题主要考查了化学方程式、影响化学反应速率的因素等知识点,难度不大,解题时注意化学实验思维的运用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.A、B、C、D、E均为有机化合物,A是分子式为C5H10O的直链化合物,B与NaHCO3溶液完全反应,其物质的量之比为1:2,它们之间的关系如图所示(提示:RCH=CHR′在酸性高锰酸钾溶液中反应生成RCOOH和R′COOH,其中R和R′为烷基).下列叙述错误的是( )
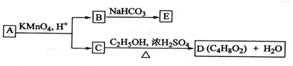

| A. | B的结构简式为HOOC-CH2-COOH | |
| B. | C与乙醇发生了酯化反应 | |
| C. | A的结构简式是CH3-CH(OH)-CH=CH-CH3 | |
| D. | E的分子式为C3H2O4Na2 |
19.下列所述的两者是同种物质的是( )
| A. | HCl和盐酸 | B. | 干冰和CO2 | C. | 正丁烷和异丁烷 | D. | 白磷和红磷 |
9.下列关于化学用语的表述正确的是(( )
| A. | 碳-14核素:${\;}_8^{14}C$ | B. | Ca2+的结构示意图为  | ||
| C. | 氮气的电子式 | D. | HCIO的结构式为H-Cl-O |
16.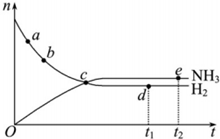 对于体积不变密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
对于体积不变密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
 对于体积不变密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
对于体积不变密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )| A. | a点、b点的正反应速率比逆反应速率大 | |
| B. | c点时每断裂3molH-H则断裂6molN-H | |
| C. | d点(t1时刻)和点e(t2时刻)处n(N2)不一样 | |
| D. | v(N2):V (NH3)=1:2时达到平衡 |
13.下列离子方程式书写不正确的是( )
| A. | 碳酸氢钠溶液与少量氢氧化钙溶液混合:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| B. | 用石墨做电极电解硫酸铜溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | |
| C. | 向FeBr2溶液中通入等量的Cl2:2Br-+2Fe2++2Cl2═Br2+2Fe3++4Cl- | |
| D. | 向硫酸铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
14.分子式为C3H4O2,能与NaOH溶液反应但不能发生加成反应的有机物(不含立体异构)有( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
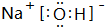 ;
;