题目内容
6.Na+的浓度不是1mol/L的溶液是( )| A. | 0.5mol/L的NaCl | B. | 0.5 mol/L的Na2SO4 | ||
| C. | 1mol/L的NaOH | D. | 0.5 mol/L的Na2CO3 |
分析 电解质离子的浓度=电解质浓度×电解质电离出该离子的数目,与溶液的体积无关,据此结合选项判断.
解答 解:A、0.5mol/L的氯化钠溶液中钠离子浓度为0.5mol/L×1=0.5mol/L,故A正确;
B、0.5mol/L的硫酸钠溶液中钠离子的浓度为0.5mol/L×2=1mol/L,故B错误;
C、1mol/L的NaOH溶液中钠离子的浓度为1mol/L×1=1mol/L,故C错误;
D、0.5mol/L的碳酸钠溶液中钠离子的浓度为0.5mol/L×2=1mol/L,故D错误.
故选A.
点评 本题考查了物质的量浓度,题目难度不大,注意掌握电解质溶液中离子的浓度与电解质浓度的计算方法,试题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
16. 25℃时,三种酸的电离平衡常数如表所示.
25℃时,三种酸的电离平衡常数如表所示.
回答下列问题:
(1)亚磷酸(H3PO3) 为二元中强酸,具有较强的还原性,可将银离子还原成银单质,在空气可缓慢氧化成H3PO4.H3PO3的电离方程式为H3PO3?H2PO3-+H+(H2PO3-?HPO32-+H+).
(2)物质的量浓度均为0.1mol•L-1的三种溶液:a.CH3COONa b.NaClO c.NaHPO3
它们的pH由小到大排列顺序是b>c>a(用字母表示).
(3)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是A(填字母).
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
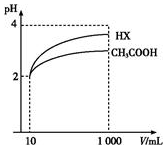
(4)体积为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的平衡常数.
 25℃时,三种酸的电离平衡常数如表所示.
25℃时,三种酸的电离平衡常数如表所示.| 化学式 | CH3COOH | HClO | H3PO3 |
| 名称 | 醋酸 | 次氯酸 | 亚磷酸 |
| 电离平衡常数(25℃) | 1.8×10-5 | 3.0×10-8 | K1=8.3×10-3 K2=5.6×10-6 |
(1)亚磷酸(H3PO3) 为二元中强酸,具有较强的还原性,可将银离子还原成银单质,在空气可缓慢氧化成H3PO4.H3PO3的电离方程式为H3PO3?H2PO3-+H+(H2PO3-?HPO32-+H+).
(2)物质的量浓度均为0.1mol•L-1的三种溶液:a.CH3COONa b.NaClO c.NaHPO3
它们的pH由小到大排列顺序是b>c>a(用字母表示).
(3)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是A(填字母).
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(4)体积为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的平衡常数.
17.X、Y、Z、W、Q五种短周期元素在元素周期表中的位置如表所示,其中X元素原子的最外层电子数是最内层电子数的3倍,则下列说法一定正确的是( )
| X | Y | |
| Z | W | Q |
| A. | X、W能分别与钠形成摩尔质量相同且阴、阳离子个数比为1:2的化合物 | |
| B. | X和Z只能形成一种化合物 | |
| C. | 氧化物对应的水化物酸性:W<Q | |
| D. | 原子半径大小关系:Q>W>Z>Y |
14.下列各选项中符合条件的同分异构体种类最多的是(均不考虑立体异构)( )
| A. | 异丁烷的二氯代物 | |
| B. | 分子式为C6 H14的有机物 | |
| C. | 甲酸正丙酯属于酯的同分异构体 | |
| D. | 分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机物 |
1. 向含MgCl2和CuCl2的溶液中逐滴加入0.1mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
向含MgCl2和CuCl2的溶液中逐滴加入0.1mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
 向含MgCl2和CuCl2的溶液中逐滴加入0.1mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
向含MgCl2和CuCl2的溶液中逐滴加入0.1mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )| A. | 原溶液中MgCl2和CuCl2的物质的量浓度相等 | |
| B. | 该实验不能证明Cu(OH)2的Ksp比Mg(OH)2的Ksp小 | |
| C. | 水的电离程度:A>B>C | |
| D. | 若向Mg(OH)2悬浊液中加入CuCl2溶液,一定会有Cu(OH)2生成 |
11.实验现象描述错误的是( )
| A. | 碘单质受热升华:紫色蒸气 | B. | 硫磺在氧气中燃烧:蓝紫色的火焰 | ||
| C. | 铁丝在氯气中燃烧:棕褐色的烟 | D. | 氢气在氯气中燃烧:淡蓝色火焰 |
2.某溶液中含有较大量的Ba2+、Cu2+、Ag+等3种阳离子,如果只取一次该溶液就能够分别将3种阳离子逐一沉淀分离出来,下列实验操作顺序正确的是( )
①滴加过量的硫酸钠溶液 ②过滤 ③滴加过量的碳酸钠溶液 ④滴加过量的盐酸.
①滴加过量的硫酸钠溶液 ②过滤 ③滴加过量的碳酸钠溶液 ④滴加过量的盐酸.
| A. | ①②④②③ | B. | ①②③②④ | C. | ④②①②③ | D. | ④②③②① |
20.向分别含1molNaOH和1molBa(OH)2的混合溶液中通入amolCO2,下列说法不正确的是( )
| A. | 当a=1.0时,反应的离子方程式为:Ba2++2OH-+CO2═BaCO3↓+H2O | |
| B. | 当a=1.5时,反应的离子方程式为:2Ba2++6OH-+3CO2═2BaCO3↓+CO32-+3H2O | |
| C. | 当a=2.5时,反应的离子方程式为:OH-+CO2═HCO3- | |
| D. | 当a=1.75时,溶液中HCO3与CO32-的物质的量之比为2:1 |