题目内容
19.实验室用二氧化锰跟浓盐酸反应制取氯气:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+MnCl2+2H2O
若计算制取的氯气为0.56L(标准状况),求:所消耗氯化氢的物质的量;被氧化的HCl物质的量.
分析 根据方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O 计算消耗MnO2的质量;被氧化的HCl生成Cl2,再根据Cl原子守恒计算.
解答 解:设制取的氯气为0.56升(标况下)需要MnO2的质量为xg,则:
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O
87g 22.4L
x g 0.56L
87g:x g=22.4L:0.56L
解得:x=2.175g;
0.56L氯气的物质的量为=$\frac{0.56L}{22.4L/mol}$=0.025mol,被氧化的HCl生成Cl2,根据Cl原子守恒可知,被氧化的HCl的物质的量为:0.025mol×2=0.05mol,
答:消耗MnO2的质量为2.175g,被氧化的HCl的物质的量为0.05mol.
点评 本题考查化学方程式有关计算、氧化还原反应的相关计算,题目难度中等,明确发生反应实质为解答关键,注意(2)中结合化合价的变化利用原子守恒计算,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
5.下列实验操作和现象,得出的结论正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用湿润的蓝色石蕊试纸检验某气体 | 试纸变红 | 气体呈碱性 |
| B | 铁粉中加入新制氯水,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 铁粉被氧化成Fe3+ |
| C | 向Mg(OH)2的上层清液中滴加MgCl2溶液 | 沉淀变成白色 | Qc[Mg(OH)2]<Ksp[Mg(OH)2] |
| D | 将少量溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CC14,振荡静置 | 下层分别为无色和紫红色 | 氧化性:Br2>Fe3+>I2 |
| A. | A | B. | B | C. | C | D. | D |
6.Na+的浓度不是1mol/L的溶液是( )
| A. | 0.5mol/L的NaCl | B. | 0.5 mol/L的Na2SO4 | ||
| C. | 1mol/L的NaOH | D. | 0.5 mol/L的Na2CO3 |
14.78gNa2O2和78gAl(OH)3分别与足量稀硫酸反应,反应后,将溶液的体积均稀释为2L,测得稀释后的两种溶液中c(H+)=0.5mol•L-1.则得到的硫酸钠溶液和硫酸铝溶液中SO42-的物质的量浓度之比为( )
| A. | 1:1 | B. | 3:4 | C. | 2:1 | D. | 3:2 |
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,22.4L CO2所含的原子数为3NA | |
| B. | 0.5mol C2H2和C6H6的气态混合物中所含原子总数为2NA | |
| C. | 1mol Cl2与足量的Fe完全反应,转移的电子数为2NA | |
| D. | 2L1mol/L的盐酸中所含HCl的分子数约为2NA |
11.25℃时,有pH=4的稀盐酸、氯化铵两种溶液和pH=10的氢氧化钠、碳酸钠两种溶液,设四种溶液中水的电离度依次为α1、α2、α3、α4.下列说法正确的是( )
| A. | α1=α2<α3=α4 | B. | α1=α3<α2=α4 | C. | α1>α2>α3>α4 | D. | α1=α4>α2=α3 |
8.根据下列烃的结构式,推断不与异丁烷互为同系物的是( )
| A. |  | B. | 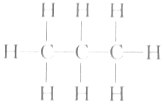 | ||
| C. |  | D. | 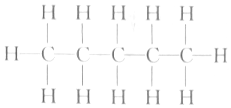 |
9.下列各组中的离子,能在溶液中大量共存的是( )
| A. | Fe2+、H+、SO42-、MnO4- | B. | Al3+、Na+、Cl-、AlO2- | ||
| C. | Ba2+、Na+、HCO3-、Cl- | D. | Fe3+、Mg2+、SCN-、Cl- |