��Ŀ����
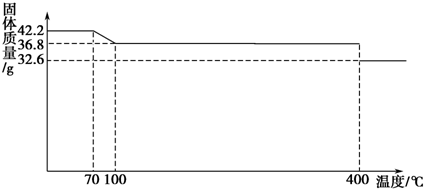
15��������������FeC6H6O7����һ�������յĸ�Ч���Ƽ��������̷���FeSO4•7H2O��ͨ�����з�Ӧ�Ʊ���FeSO4+Na2CO3�TFeCO3��+Na2SO4��FeCO3+C6H8O7�TFeC6H6O7+CO2��+H2O���±��г�����ؽ������������������������pH����ʼ������pH����������Ũ��Ϊ1.0mol•L-1���㣩��
| �������� | ��ʼ������pH | ������ȫ��pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
a����FeSO4��Һ��Na2CO3��Һͬʱ���뵽��Ӧ������
b����FeSO4��Һ�������뵽ʢ��Na2CO3��Һ�ķ�Ӧ������
c����Na2CO3��Һ�������뵽ʢ��FeSO4��Һ�ķ�Ӧ������
��2�����ɵ�FeCO3�����辭���ϴ�ӣ�����ϴ���Ƿ���ȫ�ķ�����ȡ���һ�ε�ϴ����Һ1��2mL���Թ��У������еμ��������ữ��BaCl2��Һ�����ް�ɫ�����������������ϴ�Ӹɾ���
��3�����Ƶõ�FeCO3���뵽������������Һ�У��ټ����������ۣ�80���½��跴Ӧ��
�����۵������Ƿ�ֹ+2�۵���Ԫ�ر�������
�ڷ�Ӧ������������ˣ���ȥ�������۵ķ����Ǽ������������������۷�Ӧ��ȫ��
��4�������Һ��Ũ��������������ˮ�Ҵ������á����ˡ�ϴ�ӡ��������������������壮��������м�����ˮ�Ҵ���Ŀ���ǽ���������������ˮ�е��ܽ����������ھ���������
���� �������ø��ֽⷴӦԭ������FeSO4��Na2CO3�Ƶ�FeCO3�����������ᷴӦ����������������������FeCO3 ʱҪ����Na2CO3�Լ��ԣ�ֻ�ܽ�Na2CO3��Һ�������뵽FeSO4��Һ�У������������Fe��OH��2������Ϊ�Ʊ����������������������뽫Na2CO3ϴ�Ӹɾ�����ȥ���溬��SO42-�IJ�����Һ��ͬʱ���������з�ֹ+2�������������������������Ҫ�ӷ�Ӧ���Һ�з������ʱ��ͨ������Ũ���ᾧ�ķ����õ���
��1������Na2CO3��Һ��FeSO4��Һ��Ӧ�Ʊ�FeCO3������Na2CO3��Һ���Ժ�ǿ�����ܻ�����Fe��OH��2������Ϊ��������Fe��OH��2�����������Na2CO3����FeSO4��Һ�У�Fe2+�ǹ����ģ�����FeSO4��ҺΪ���ԣ�Fe2+���׳�������ˣ�CO32-������Fe2+���Ϊ�������������Ӧ��Na2CO3��Һ�������뵽ʢ��FeSO4��Һ�ķ�Ӧ�����У�
��2���жϳ����Ƿ�ϴ���ķ�����ȡ���һ��ϴ�ӵ���Һ�������Һ���Ƿ����δϴ�Ӹɾ������ʣ�����ҪŪ������ϵ�������ʲô��Ȼ����ȥ�����������ӣ�������FeCO3���Ʊ�����Na2CO3��Һ��FeSO4��Һ�ķ�Ӧ���������������ܻ���Na2SO4���ʣ����Ӧ�ü������һ��ϴ����Һ���Ƿ���SO42-���������ת����SO42-�ļ��飻
��3����+2��FeԪ���ױ������е������������Ʊ�����������������Ӧ���������������Ӵ����������۵�Ŀ�ľ����������ᷴӦ����H2���γ�һ�������Ļ�������ȥ���������ۿ�ֱ�Ӽ��������������ᣬ��ӦҲ��������Ҫ�IJ�Ʒ�����������������������ʣ�
��4��������Һ��Ũ���γ������������ı�����Һ��Ҫ�õ������ܶ���������������壬�ɼ�����ˮ�Ҵ������Խ����������������ܽ�ȣ��Ӷ���ø���IJ�Ʒ��
��� �⣺��1������Na2CO3��Һ��FeSO4��Һ��Ӧ�Ʊ�FeCO3������Na2CO3��Һ���Ժ�ǿ�����ܻ�����Fe��OH��2�����������Na2CO3����FeSO4��Һ�У�Fe2+�ǹ����ģ�����FeSO4��ҺΪ���ԣ�Fe2+���׳�������ˣ�CO32-������Fe2+���Ϊ�������������Ϊ��������Fe��OH��2������Ӧ��Na2CO3��Һ�������뵽ʢ��FeSO4��Һ�ķ�Ӧ�����У��ʴ�Ϊ��c����������Fe��OH��2������
��2��Na2CO3���溬��SO42-�IJ�����Һ��ֻҪϴ��Һ����鲻��SO42-������֤��ϴ�Ӹɾ������������ȡ���һ��ϴ�ӵ���Һ��1��2 mL ���Թ��У������еμ��������ữ��BaCl2��Һ�����ް�ɫ�����������������ϴ�Ӹɾ���
�ʴ�Ϊ��ȡ���һ�ε�ϴ����Һ1��2 mL ���Թ��У������еμ��������ữ��BaCl2��Һ�����ް�ɫ�����������������ϴ�Ӹɾ���
��3����+2��FeԪ���ױ������е������������Ʊ�����������������Ӧ���������������Ӵ����������۵�Ŀ�ľ����������ᷴӦ����H2���γ�һ�������Ļ�������ȥ���������ۿ�ֱ�Ӽ��������������ᣬ��ӦҲ��������Ҫ�IJ�Ʒ�����������������������ʣ�
�ʴ�Ϊ����ֹ+2�۵���Ԫ�ر��������������������������۷�Ӧ��ȫ��
��4��������Һ��Ũ���γ������������ı�����Һ��Ҫ�õ������ܶ���������������壬�ɼ�����ˮ�Ҵ������Խ����������������ܽ�ȣ��Ӷ���ø���IJ�Ʒ��
�ʴ�Ϊ������������������ˮ�е��ܽ����������ھ���������
���� ���⿼����ѧ�������龳�����ʵ��Ʊ�ʵ���л�����ʵ�鼼�ܺͶԽ̲����ʵ��������Ǩ���������е����Ѷ�ƫ�������������ʺ�ʵ�鼼���ǽ���ؼ���

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | CH4 | B�� | C2H6 | C�� | C2H2 | D�� | C3H4 |
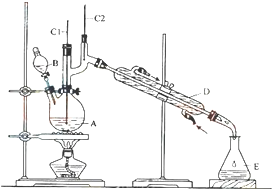 ����ȩ��һ�ֻ���ԭ�ϣ�ijʵ��С��������ͼװ�úϳ�����ȩ�������ķ�Ӧ���£�
����ȩ��һ�ֻ���ԭ�ϣ�ijʵ��С��������ͼװ�úϳ�����ȩ�������ķ�Ӧ���£�CH3CH2CH2CH2OH $��_{H_{2}SO_{4}����}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
��Ӧ��Ͳ������������б����£�
| �е�/0C | �ܶ�/��g•cm-3�� | ˮ���ܽ��� | |
| ������ | 117.2 | 0.8109 | �� |
| ����ȩ | 75.7 | 0.8017 | �� |
��6.0gNa2Cr2O7����100mL�ձ��У���30mLˮ�ܽ⣬�ٻ�������5mLŨ���ᣬ��������ҺС��ת����B�У���A�м���4.0g�������ͼ�����ʯ�����ȣ�������������ʱ����ʼ�μ�B����Һ���μӹ����б��ַ�Ӧ�¶�Ϊ90-95�棬��E���ռ�90�����µ���֣�������ﵹ���Һ©���У���ȥˮ�㣬�л������������ռ�75-77����֣�����2.0g��
�ش��������⣺
��1��ʵ���У��ܷ�Na2Cr2O7��Һ�ӵ�Ũ�����У�˵�����ɲ��ܣ�Ũ��������ˮ�ų������ȣ��������Ž����ˣ�
��2�������ʯ�������Ƿ�ֹ����
��3������װ��ͼ�У�B�����������Ƿ�Һ©����D������������ֱ�������ܣ�
��4����Һ©��ʹ��ǰ������еIJ�����c������ȷ�𰸱�ţ���
a����ʪ b������ c����© d���궨
��5��������ȩ�ֲ�Ʒ���ڷ�Һ©���з�ˮʱ��ˮ���²㣨��ϡ����¡���
��6����Ӧ�¶�Ӧ������90-95�棬��ԭ���ǣ���֤����ȩ��ʱ��������ʹ��Ӧ������У��ֿɾ��������䱻��һ������
��7����ʵ���У�����ȩ�IJ���Ϊ51%
��8����֪����ȩ�ڼ��������¿��Ա�����������ͭ������д���÷�Ӧ�Ļ�ѧ����ʽ��CH3CH2CH2CHO+NaOH+2Cu��OH��2$\stackrel{��}{��}$CH3CH2CH2COONa+Cu2O��+3H2O��