题目内容
15.下列物质间的相互转化,相邻两种物质的转化可通过一步反应就能实现的是( )| A. | Si→SiO2→H2SiO3→Na2SiO3 | B. | C→CO2→CaCO3→CO2→C | ||
| C. | Al→Al2O3→Al(OH)3→NaAlO2 | D. | FeCO3→FeO→Fe(OH)2→Fe(OH)3→Fe2O3 |
分析 A.SiO2不能一步反应生成硅酸;
B.碳和氧气反应生成二氧化碳,二氧化碳和氢氧化钙溶液反应生成碳酸钙,碳酸钙分解生成二氧化碳,二氧化碳和碳高温反应生成一氧化碳;
C.氧化铝不能一步反应生成氢氧化铝;
D.转化关系中氧化亚铁不能一步反应生成氢氧化亚铁.
解答 解:A.Si$\stackrel{O_{2}}{→}$SiO2不能直接反应生成H2SiO3,故A错误;
B.C$\stackrel{O_{2}}{→}$CO2$\stackrel{Ca(OH)_{2}}{→}$CaCO3$\stackrel{△}{→}$CO2$\stackrel{C}{→}$C,可通过一步反应就能实现,故B正确;
C.Al$\stackrel{O_{2}}{→}$Al2O3不能一步实现反应生成Al(OH)3,故C错误;
D.FeCO3$\stackrel{△}{→}$FeO不能一步反应生成Fe(OH)2,故D错误;
故选B.
点评 本题考查了物质现在、物质组成、物质转化的分析应用,掌握基础是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.对反应BrF3+H2O-Br2+HBrO3+O2↑+HF(未配平),下列说法不正确的是( )
| A. | Br2和HBrO3均是氧化产物 | |
| B. | BrF3既是氧化剂,又是还原剂 | |
| C. | BrF3的氧化性强于O2 | |
| D. | 反应中,若生成1molBr2,则反应转移6NA个电子 |
7.共价键都有键能之说,键能是指拆开1mol共价键所需要吸收的能量或生成1mol共价键所能够放出的能量.如H-H键的键能是指1mol H2分子变成2mol H原子需要吸收436KJ的能量或2mol H原子变成1mol H2分子能够放出436KJ的能量.
(1)已知H-Cl键的键能为431.4kJ/mol,下列关于键能的叙述正确的是AD
A.每生成1molH-Cl键放出431.4kJ能量
B.每生成1molH-Cl键吸收431.4kJ能量
C.每拆开1molH-Cl键放出431.4kJ能量
D.每拆开1mol H-Cl键吸收431.4kJ能量
(2)参考表中的数据,判断下列分子受热时最稳定的是A
A、HF B、HCI C、HBr D、H2
(3)能用键能大小解释的是A
A、氮气的化学性质比氧气稳定
B、常温常压下,溴呈液态,碘呈固态
C、稀有气体一般很难发生化学反应
D、硝酸易挥发而硫酸难挥发.
(1)已知H-Cl键的键能为431.4kJ/mol,下列关于键能的叙述正确的是AD
A.每生成1molH-Cl键放出431.4kJ能量
B.每生成1molH-Cl键吸收431.4kJ能量
C.每拆开1molH-Cl键放出431.4kJ能量
D.每拆开1mol H-Cl键吸收431.4kJ能量
(2)参考表中的数据,判断下列分子受热时最稳定的是A
| 化学键 | H-H | H-F | H-Cl | H-Br |
| 键能kJ/mol | 436 | 565 | 431 | 368 |
(3)能用键能大小解释的是A
A、氮气的化学性质比氧气稳定
B、常温常压下,溴呈液态,碘呈固态
C、稀有气体一般很难发生化学反应
D、硝酸易挥发而硫酸难挥发.
4.下列分子式表示的各物质中,属于烃的是( )
| A. | C2H6O | B. | C6H6 | C. | HCN | D. | CO(NH2)2 |
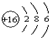 ;该元素最高正化合价与最低负化合价分别是+6和-2.
;该元素最高正化合价与最低负化合价分别是+6和-2.
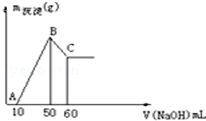 把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入1mol•L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示,回答下列问题,要求写出计算过程.
把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入1mol•L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示,回答下列问题,要求写出计算过程.
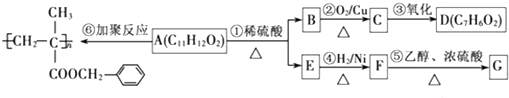
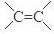 、-COOH;F的名称2-甲基丙酸(系统命名法命名).
、-COOH;F的名称2-甲基丙酸(系统命名法命名).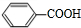 .
.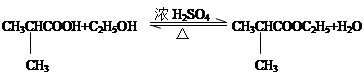 .⑤的反应类型是酯化反应(或取代反应).
.⑤的反应类型是酯化反应(或取代反应).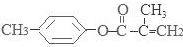 .
.