题目内容
(1)在恒温恒压容器中开始时放入1molA和1molB到达平衡后生成amol C,若维持温度不变,在一个与(1)反应(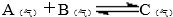 )前起始体积相同、且容积固定的容器中发生上述反应开始时放入1mol A和1mol B到达平衡后生成bmol C.将b与(1)小题中的a进行比较 (先填一个编号)(甲)a<b(乙) a>b(丙) a=b(丁)不能比较a和b的大小作出此判断的理由是 .
)前起始体积相同、且容积固定的容器中发生上述反应开始时放入1mol A和1mol B到达平衡后生成bmol C.将b与(1)小题中的a进行比较 (先填一个编号)(甲)a<b(乙) a>b(丙) a=b(丁)不能比较a和b的大小作出此判断的理由是 .
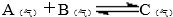 )前起始体积相同、且容积固定的容器中发生上述反应开始时放入1mol A和1mol B到达平衡后生成bmol C.将b与(1)小题中的a进行比较
)前起始体积相同、且容积固定的容器中发生上述反应开始时放入1mol A和1mol B到达平衡后生成bmol C.将b与(1)小题中的a进行比较考点:化学平衡的影响因素
专题:化学平衡专题
分析:依据恒温恒压容器、恒温恒容容器中的压强对平衡影响进行分析判断解题.
解答:
解:在恒温恒压容器中开始时放入1molA和1molB到达平衡后生成amol C;在恒温恒容容器中开始时放入1molA和1molB到达平衡后生成b molC;反应A(g)+B(g)?C(g)是气体体积减少的反应,在恒温恒容容器中,随反应进行压强减小,在恒温恒压容器中随反应进行,过程中的压强为保持恒压,体积减小,所以本小题的容器中的压力小于(1)小题容器中的压力,有利于逆向反应,因此平衡后b<a;
故答案为:乙;因为本小题中容器容积不变,而(1)小题中容器的容积缩小,所以本小题的容器中的压力小于(1)小题容器中的压力,有利于逆向反应.
故答案为:乙;因为本小题中容器容积不变,而(1)小题中容器的容积缩小,所以本小题的容器中的压力小于(1)小题容器中的压力,有利于逆向反应.
点评:本题考查了等效平衡的分析应用和判断,充分利用各步的隐含条件,依据等效平衡的特征分析是本题的关键,区分恒温恒容容器和恒温恒压容器的不同.题目较难,但抓住实质会较易解决.

练习册系列答案
相关题目
下列能达到实验目的是( )
A、 吸收HCl防倒吸 |
B、 制取少量蒸馏水 |
C、 CaCO3和稀硫酸制取CO2 |
D、 除去杂质气体CO2 |
下列说法中,正确的是( )
| A、铅笔芯的主要成分是金属铅,儿童在使用是不可用嘴吮吸,以免引起铅中毒 |
| B、CO有毒,在生有炉火的居室中多放几盆水,可吸收CO,防止煤气中毒 |
| C、含氟冰箱产生的氟利昂是造成臭氧空洞的主要原因 |
| D、油条制作中常加入明矾作膨化剂,有利于补充身体所需微量元素,是理想早餐 |
用铂电极电解CuCl2与CuSO4的混合溶液(浓度均为2mol/L)50mL,当阴极析出9.6g固体时,标准状况下阳极得到的气体是( )
| A、2.24L | B、2.8L |
| C、3.36L | D、4.48L |
1.52g 铜镁合金完全溶解于50mL 密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
| A、该合金中铜与镁的物质的量之比是2:1 |
| B、得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL |
| C、NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D、该浓硝酸中HNO3的物质的量浓度是14.0 mol/L |
下列实验操作中,主要不是从安全因素考虑的是( )
| A、点燃氢气前一定要检验氢气的纯度 |
| B、未使用完的白磷要随时收集起来,并与空气隔绝 |
| C、用氢气还原氧化铜时,要先通一会儿氢气,再加热氧化铜 |
| D、酒精灯不用时,必须盖上灯帽 |
下列固体混合物与过量的稀H2SO4反应,能产生气泡并有沉淀生产的是( )
| A、NaHCO3和Al(OH)3 |
| B、BaCl2和NaCl |
| C、KClO3和K2SO4 |
| D、Na2SO3和BaCO3 |
 实验室需要480mL 0.4mol?L-1的NaCl溶液,有如下操作步骤:
实验室需要480mL 0.4mol?L-1的NaCl溶液,有如下操作步骤:


