题目内容
13.下列A-D四组,每组有两个反应,其中两个反应能用同一离子方程式表示的是:( )| (Ⅰ) | (Ⅱ) | |
| A | 少量H2SO4滴入Ba(OH)2溶液中 | 少量NaHSO4滴入Ba(OH)2溶液中 |
| B | 少量NaOH滴入Al2(SO4)3溶液中 | 少量Al2(SO4)3溶液滴入氨水中 |
| C | FeO与足量的盐酸 | FeO与足量的稀硝酸 |
| D | 0.1mol Cl2通入含0.2mol FeBr2的溶液中 | 0.1mol Cl2通入含0.2mol FeCl2的溶液中 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.H2SO4与Ba(OH)2反应方程式与反应物的量无关,NaHSO4与Ba(OH)2反应方程式与反应物的量有关;
B.一水合氨是弱电解质,氢氧化钠是强电解质;
C.硝酸具有强的氧化性,能够氧化二价铁离子;
D.0.1mol Cl2通入含0.2mol FeBr2的溶液中,只有亚铁离子被氧化.
解答 解:A.H2SO4与Ba(OH)2反应方程式与反应物的量无关,Ba2++2OH-+SO42-+2H+=BaSO4↓+2H2O,NaHSO4与Ba(OH)2反应方程式与反应物的量有关,少量NaHSO4滴入Ba(OH)2溶液中,Ba2++OH-+SO42-+H+=BaSO4↓+H2O,所以离子方程式不同,故A错误;
B.少量NaOH滴入Al2(SO4)3溶液中,其离子方程式为:Al3++3OH-=Al(OH)3↓,少量Al2(SO4)3溶液滴入氨水中,其离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+NH4+,所以离子方程式不同,故B错误;
C.FeO与足量的盐酸反应离子方程式:FeO+2H+=Fe2++H2O,FeO与足量的稀硝酸反应离子方程式:3FeO+10H++NO3-═3Fe3++NO↑+5H2O,故C错误;
D.0.1mol Cl2通入含0.2mol FeBr2的溶液中,只有亚铁离子被氧化,0.1mol Cl2通入含0.2mol FeCl2的溶液中,也是Cl2与亚铁离子反应,所以离子方程式相同为2Fe2++Cl2=2Fe3++2Cl-,故D正确.
故选D.
点评 本题考查离子方程式的书写,明确物质的溶解性、物质的性质及离子方程式书写规则即可解答,注意反应物用量及反应条件对反应的影响,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.在盛有硫酸铜饱和溶液的烧杯中,投入一块不规则的硫酸铜晶体,隔一段时间后,得到的结论是( )
| A. | 晶体部分溶解了 | |
| B. | 晶体形状和质量不变 | |
| C. | 晶体的质量增加了,形状也发生了改变 | |
| D. | 晶体的质量不变,形状改变了 |
1.CuI是一种白色不溶于水的固体,以石墨(阴)和铜(阳)为电极组成电解槽,以含酚酞和淀粉的KI水溶液为电解液进行电解.电解开始不久,阴极区溶液显红色,而阳极区仍为无色.过了相当长的时间后,阳极区才呈蓝色,则电解开始时的电极反应为( )
| A. | 阳极反应:Cu-2e-═Cu2+ 阴极反应:Cu2++2e-═Cu | |
| B. | 阳极反应:2Cu-2e-+2I-═2CuI 阴极反应:2H++2e-═H2↑ | |
| C. | 阳极反应:2I--2e-═I2 阴极反应:2H++2e-═H2↑ | |
| D. | 阳极反应:Cu-2e-═Cu2+ 阴极反应:2H++2e-═H2↑ |
18.在酸性溶液中能大量共存而且为无色透明的溶液是( )
| A. | NH4+、Al3+、CO32-、NO3- | B. | K+、Na+、NO3-、SO42- | ||
| C. | K+、MnO4-、NH4+、NO3- | D. | Na+、K+、HCO3-、NO3- |
2.下列有关化学反应表达正确的是( )
| A. | 实验室用液溴和苯在催化剂作用下制溴苯: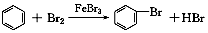 | |
| B. | 蛋壳溶于食醋:CaCO3+CH3COOH=CH3COOCa+H2O+CO2↑ | |
| C. | 甲醛溶液中加入足量新制碱性Cu(OH)2悬浊液并加热HCHO+2 Cu(OH)2+NaOH$\stackrel{△}{→}$ HCOONa+Cu2O↓+3H2O | |
| D. | 向氯乙烷水溶液中加入氢氧化钠溶液共热:CH3CH2Cl+NaOH $→_{△}^{水}$ CH2=CH2+NaCl+H2O |
3.水的状态有气态、液态、固态,还有玻璃态.玻璃态水是液态水急速冷却到165K时形成的,无固定形状,不存在晶体,且密度与普通水相同.下列有关叙述正确的是( )
| A. | 当水结成冰时,水分子间的间距会减小,因而密度增大 | |
| B. | 玻璃态水与液态水具有不同酌化学性质 | |
| C. | 玻璃态水是水的一种特殊状态 | |
| D. | 纯净水与食盐水的冰点相同 |