题目内容
15.下列各项中括号里的物质是除去杂质所用的药品,其中错误的是( )| A. | SO2中有少量HCl气体(氢氧化钠溶液) | B. | CO中混有CO2(石灰水、浓硫酸) | ||
| C. | CO2中有少量CO(灼热氧化铜) | D. | Cl2中混有HCl(饱和食盐水、浓硫酸) |
分析 A.二者都与氢氧化钠溶液反应;
B.二氧化碳可与石灰水反应;
C.CO可与CuO反应生成二氧化碳;
D.氯气不溶于饱和食盐水.
解答 解:A.二者都与氢氧化钠溶液反应,应用饱和亚硫酸氢钠溶液除杂,故A错误;
B.二氧化碳可与石灰水反应,然后用浓硫酸干燥,可得到纯净的CO,故B正确;
C.CO可与CuO反应生成二氧化碳,可用于除杂,故C正确;
D.氯气不溶于饱和食盐水,可用浓硫酸干燥,可用于除杂,故D正确.
故选A.
点评 本题考查物质的分离、提纯的基本方法选择与应用,为高频考点,题目难度中等,注意根据混合物组分性质的差异性选择分离的方法,注意加入试剂的顺序和除杂原理.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.可逆反应:2NO2?2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成nmolO2的同时生成2nmolNO2
②NO2与NO速率相等
③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
⑦混合气体的压强不再改变的状态.
①单位时间内生成nmolO2的同时生成2nmolNO2
②NO2与NO速率相等
③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
⑦混合气体的压强不再改变的状态.
| A. | ①④⑥⑦ | B. | ②③⑤ | C. | ①②④⑥⑦ | D. | ①②③④⑥⑦ |
3.下列说法中正确的是( )
| A. | 加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ca2+ | |
| B. | 某溶液与NaOH溶液共热,产生使湿润红色石蕊试纸变蓝气体,说明原溶液中存在NH4+ | |
| C. | 某溶液加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,则一定含有CO32- | |
| D. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
10.下列物质发生变化时,所克服的粒子间相互作用属于分子间作用力的是( )
| A. | 酒精受热变为气体 | B. | 氯化铵受热变为气体 | ||
| C. | 二氧化硅受热熔化 | D. | 食盐溶解在水中 |
20.现有NH4Cl、MgSO4、(NH4)2SO4和NaCl四种无色溶液,用一种试剂就可将它们鉴别出来,这种试剂是( )
| A. | NaOH | B. | Ba(OH)2 | C. | AgNO3 | D. | HCl |
7.大力开发低碳技术,推广高效节能技术,积极发展新能源和可再生能源.下列有关做法与此不相符的是( )
| A. | 回收废弃的饮料包装纸,制作成公园内的休闲长椅 | |
| B. | 大力开发丰富的煤炭资源,减少对石油的依赖 | |
| C. | 在西部和沿海地区兴建风力发电站,解决能源问题 | |
| D. | 鼓励购买小排量汽车,推广电动、混合动力汽车 |
18.下列根据反应原理设计的应用,不正确的是( )
| A. | CO32-+H2O?HCO3-+OH-:用热的纯碱溶液清洗油污 | |
| B. | A13++3H2O?AI(OH)3(胶体)+3H+:明矾净水 | |
| C. | SnCl2+H2O?Sn( OH)Cl↓+HCl配制氯化亚锡溶液时加入氢氧化钠溶液 | |
| D. | TiCl4+(x+2)H2O(过量)?TiO2•xH2O↓+3H+:制备TiO2纳米粉 |
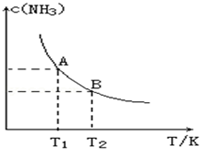 在一定条件下,将1.00molN2(g)与3.00molH2(g)混合于一个10.0L密闭容器中,在不同温度下达到平衡时NH3(g)的平衡浓度如图所示.其中温度为T1时平衡混合气体中氨气的体积分数为25.0%.
在一定条件下,将1.00molN2(g)与3.00molH2(g)混合于一个10.0L密闭容器中,在不同温度下达到平衡时NH3(g)的平衡浓度如图所示.其中温度为T1时平衡混合气体中氨气的体积分数为25.0%.