题目内容
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A、0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-) | ||
| B、0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7):c(NH3?H2O)>c(NH4+)>c(Cl-)>c(OH-) | ||
C、0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:
| ||
| D、0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:A、0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合反应生成NaCl和CH3COOH,醋酸是弱电解质存在电离平衡,溶液呈酸性;
B、0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7),说明溶液中一水合氨电离大于铵根离子水解溶液呈碱性;
C、结合混合溶液中物料守恒分析判断;
D、结合反应后溶液中电荷守恒分析判断.
B、0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7),说明溶液中一水合氨电离大于铵根离子水解溶液呈碱性;
C、结合混合溶液中物料守恒分析判断;
D、结合反应后溶液中电荷守恒分析判断.
解答:
解:A、0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合反应生成NaCl和CH3COOH,醋酸是弱电解质存在电离平衡,溶液呈酸性,溶液中离子浓度c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-),故A正确;
B、0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7),说明溶液中一水合氨电离大于铵根离子水解溶液呈碱性,c(NH4+)>c(Cl-)>c(NH3?H2O)>c(OH-),故B错误;
C、0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:n(Na):n(C)=3:2,溶液中物料守恒得到:2c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)],故C正确;
D、0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸)反应生成氯化钠、NaHC2O4,溶液中存在电荷守恒为:c(Cl-)+2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+),故D错误;
故选AC.
B、0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7),说明溶液中一水合氨电离大于铵根离子水解溶液呈碱性,c(NH4+)>c(Cl-)>c(NH3?H2O)>c(OH-),故B错误;
C、0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:n(Na):n(C)=3:2,溶液中物料守恒得到:2c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)],故C正确;
D、0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸)反应生成氯化钠、NaHC2O4,溶液中存在电荷守恒为:c(Cl-)+2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+),故D错误;
故选AC.
点评:本题考查了溶液中离子浓度大小比较、盐的水解原理及其应用,题目难度中等,注意明确盐的水解原理,掌握比较溶液中离子浓度大小的方法,明确电荷守恒、物料守恒等比较离子浓度大小中应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
生活处处有化学,下列说法正确的是( )
| A、青铜、硬铝和碳素钢都是合金 |
| B、葡萄糖和蔗糖互为同分异构体 |
| C、淀粉、蛋白质和花生油都是天然高分子化合物 |
| D、食用植物油在酸性或碱性条件下水解产物相同 |
 简单原子的原子结构可用图形象地表示:其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的组合是( )
简单原子的原子结构可用图形象地表示:其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的组合是( )a.①②③互为同位素
b.①②③互为同素异形体
c.①②③是三种化学性质不同的粒子
d.①②③具有相同的质量数
e.①②③具有相同的质量
f.①②③是三种不同的原子.
| A、a、f | B、b、c |
| C、d、e | D、e、f |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、0.5 molAl与足量盐酸反应转移电子数为1NA |
| B、标准状况下,11.2L SO3所含的分子数为0.5NA |
| C、0.1molCH4所含的电子数为1NA |
| D、46gNO2和N2O4的混合物含有的分子数为1NA |
下列各组离子能够大量共存的是( )
| A、K+、Al3+、Cl-、AlO2- |
| B、Fe2+、Mg2+、SO42-、NO3- |
| C、Fe3+、K+、SO42-、S2- |
| D、Na+、Ca2+、OH-、HCO3- |
氢化热是指一定条件下,1mol不饱和化合物加氢时放出的热量.表中是环己烯( )、环己二烯(
)、环己二烯(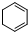 )和苯的氢化热数据:
)和苯的氢化热数据:
根据表中数据推断正确的是( )
 )、环己二烯(
)、环己二烯( )和苯的氢化热数据:
)和苯的氢化热数据:| 物质 | 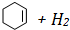 | 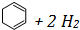 |  |
| 氢化热(kJ/mol) | 119.7 | 232.7 | 208.4 |
| A、环己二烯与H2的反应最剧烈 |
| B、环己烯、环己二烯和苯有相同的官能团 |
| C、三种化合物中环己二烯的稳定性最强 |
D、上述条件下,1 mo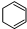 转变 转变 为时放出热量 为时放出热量 |
荧光棒发光的原理是利用H2O2氧化草酸酯产生能量,该能量传递给荧光物质而发光.草酸酯是一种粘稠度较高的有机化合物.下列说法不正确的是( )
| A、荧光棒发光,凑近可燃性气体,会导致气体燃烧 |
| B、当荧光棒亮度减弱时,敲打荧光棒亮度可能增强 |
| C、荧光棒放入冷冻室亮度可能减弱甚至消失 |
| D、荧光棒发光是化学能转化为热能,热能转化为光能 |
 下面是唐朝刘禹锡描写沙里淘金的一首诗,其中有的诗句可能包含了某一化学实验现象或化学过程,请在这样的诗句后面写出相应的文字.
下面是唐朝刘禹锡描写沙里淘金的一首诗,其中有的诗句可能包含了某一化学实验现象或化学过程,请在这样的诗句后面写出相应的文字.