题目内容
4.常温下,pH为3的FeCl3溶液,pH为11的Na2CO3溶液和pH为3的盐酸中由水电离出来的H+的浓度分别为:C1、C2、C3,它们之间的关系是( )| A. | C1<C2<C3 | B. | C1=C2>C3 | C. | C1>C2>C3 | D. | 无法判断 |
分析 FeCl3和Na2CO3都可促进水的电离,盐酸抑制电离,结合溶液的pH判断水的电离程度大小.
解答 解:FeCl3和Na2CO3都可促进水的电离,pH为3的FeCl3溶液,水电离出来的H+的浓度为10-3mol/L,pH为11的Na2CO3溶液,水电离出来的H+的浓度为10-3mol/L,
pH为3的盐酸抑制水的电离,水电离出来的H+的浓度为10-11mol/L,
则C1=C2>C3,故选B.
点评 本题考查盐类水解的应用以及弱电解质的电离等问题,为高考常见题型,综合考查学生的分析能力和综合运用化学知识的能力,注意相关基础知识的理解和积累,难度不大.

练习册系列答案
相关题目
14.下列有机物是按照碳的骨架进行分类的是( )
| A. | 烷烃 | B. | 烯烃 | C. | 芳香烃 | D. | 卤代烃 |
15.下列化合物分子中的所有碳原子可能处于同一平面的是( )
| A. | 甲基环己烷 | B. | 聚-2-甲基丙烯 | C. | 乙酸叔丁酯 | D. | 苯甲酸苯甲酯 |
16.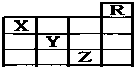 如图所示是元素周期表前四周期的一部分,关于元素X、Y、Z的叙述正确的是:( )
如图所示是元素周期表前四周期的一部分,关于元素X、Y、Z的叙述正确的是:( )
①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐
②同浓度X、Y、Z的气态氢化物水溶液的pH:X>Y>Z
③Z的单质在常温下是液体,可与铁粉反应
④Z的原子序数比Y大19.
 如图所示是元素周期表前四周期的一部分,关于元素X、Y、Z的叙述正确的是:( )
如图所示是元素周期表前四周期的一部分,关于元素X、Y、Z的叙述正确的是:( )①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐
②同浓度X、Y、Z的气态氢化物水溶液的pH:X>Y>Z
③Z的单质在常温下是液体,可与铁粉反应
④Z的原子序数比Y大19.
| A. | ③ | B. | ①②③④ | C. | ①④ | D. | ①② |
13.下列各组指定的元素,不能形成AB2型化合物的是( )
| A. | 2s22p2 和2s22p4 | B. | 3s23p4 和2s22p4 | C. | 3s2和2s22p5 | D. | 3s1和3s23p5 |
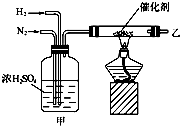 实验室合成氨的装置如图所示.
实验室合成氨的装置如图所示.