题目内容
如图中A~I都是中学化学中常见的物质.已知A、D、G为单质,其余为化合物,B是一种红棕色的固体.
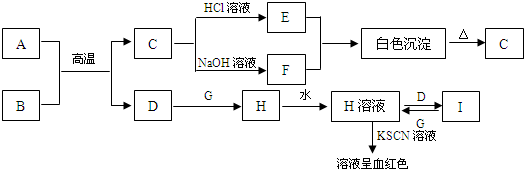
回答下列问题:
(1)写出F的化学式 .
(2)写出组成单质G的元素在周期表中的位置 .
(3)写出A+B→C+D的化学方程式: .
(4)写出I+G→H的离子方程式: .

回答下列问题:
(1)写出F的化学式
(2)写出组成单质G的元素在周期表中的位置
(3)写出A+B→C+D的化学方程式:
(4)写出I+G→H的离子方程式:
考点:无机物的推断
专题:推断题
分析:B是一种红棕色的固体,应为Fe2O3,与单质A反应生成化合物C与单质D,则D为Fe,C为氧化物,既与盐酸反应又能与氢氧化钠反应,C应为Al2O3,则A是Al,E为AlCl3,F为NaAlO2,氯化铝与偏铝酸钠反应得到白色沉淀为Al(OH)3,加热分解得到氧化铝.G为单质,与Fe反应得到H,H的溶液与KSCN溶液反应,溶液呈红色,H含有Fe3+,则G为Cl2,H为FeCl3,H与D反应得到I为FeCl2,FeCl2与氯气反应可以得到FeCl3,结合元素化合物的性质解答.
解答:
解:B是一种红棕色的固体,应为Fe2O3,与单质A反应生成化合物C与单质D,则D为Fe,C为氧化物,既与盐酸反应又能与氢氧化钠反应,C应为Al2O3,则A是Al,E为AlCl3,F为NaAlO2,氯化铝与偏铝酸钠反应得到白色沉淀为Al(OH)3,加热分解得到氧化铝.G为单质,与Fe反应得到H,H的溶液与KSCN溶液反应,溶液呈红色,H含有Fe3+,则G为Cl2,H为FeCl3,H与D反应得到I为FeCl2,FeCl2与氯气反应可以得到FeCl3,
(1)由上述分析可知,F的化学式为,故答案为:NaAlO2;
(2)单质G为Cl2,Cl元素在周期表中的位置为:第三周期第ⅦA族,故答案为:第三周期第ⅦA族;
(3)A+B→C+D的化学方程式为:Fe2O3+2Al
A12O3+2Fe,故答案为:Fe2O3+2Al
A12O3+2Fe;
(4)I+G→H的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-.
(1)由上述分析可知,F的化学式为,故答案为:NaAlO2;
(2)单质G为Cl2,Cl元素在周期表中的位置为:第三周期第ⅦA族,故答案为:第三周期第ⅦA族;
(3)A+B→C+D的化学方程式为:Fe2O3+2Al
| ||
| ||
(4)I+G→H的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-.
点评:本题考查无机物的推断,题目难度中等,B的颜色及转化关系中特殊反应是推断突破口,再结合转化关系与进行推断,侧重考查元素化合物性质,学习中注意把握.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
“绿色化学”要求综合考虑经济、技术、环保等方面来设计化学反应线路.下列各反应路线符合“绿色化学”思想的是( )
A、制CuSO4:Cu+2H2SO4(浓)
| ||||
B、制CuSO4:2Cu+O2
| ||||
| C、制Cu(NO3)2:Cu+4HNO4(浓)=Cu(NO3)2+2NO2↑+2H2O | ||||
| D、制Cu(NO3)2:3Cu+8HNO4(浓)=3Cu(NO3)2+2NO↑+4H2O |
以下有机物的结构简式正确的是( )
| A、甲醛HCOH |
B、苯酚 |
| C、硬脂酸钠C17H35COONa |
D、3,3-二甲基丁烷 |
下列做法正确的是( )
| A、钠着火时用沙子扑灭 |
| B、点燃氢气前要验纯,点燃甲烷前无需验纯 |
| C、氨气泄漏时,用湿毛巾捂住口鼻,并尽量向高处去 |
| D、少量浓硫酸沾在皮肤上,立即用大量氢氧化钠溶液冲洗 |
在高温、高压和催化剂条件下的密闭容器中,进行反应:N2(g)+3H2(g)?2NH3(g)(正反应放热).下列有关说法不正确的是( )
| A、使用催化剂是为了增大化学反应速率 |
| B、增大氢气的浓度可增大反应速率 |
| C、在上述条件下,氢气能全部转化为氨气 |
| D、达到平衡时,体系中各物质的浓度不再改变 |
