题目内容
某温度时,在2L密闭容器中气态物质CO和H2反应生成气态物质Z,它们的物质的量随时间的变化如下表所示.
(1)(根据上表中数据,在图1中画出CO、Z的物质的量的浓度(c)随时间(t)变化的曲线:

(2)体系中发生反应的化学方程式是 .
(3)在3-5min时间内产物Z的平均反应速率: .
(4)图2表示该反应进行过程中能量的变化.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.该反应是 (填“吸热”或“放热”)反应,反应的热化学方程式是 .
(5)恒容条件下,下列措施中能使n(CH3OH)/n(CO)增大的有 (选填序号).
a.升高温度 b.使用催化剂 C.再充入2mol H2 d.再充入2mol He.
| t/min | CO/mol | H2/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.10 |
| 3 | 0.75 | 0.50 | 0.25 |
| 5 | 0.65 | 0.30 | 0.35 |
| 7 | 0.55 | 0.10 | 0.45 |
| 9 | 0.55 | 0.10 | 0.45 |
| 10 | 0.55 | 0.10 | 0.45 |

(2)体系中发生反应的化学方程式是
(3)在3-5min时间内产物Z的平均反应速率:
(4)图2表示该反应进行过程中能量的变化.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.该反应是
(5)恒容条件下,下列措施中能使n(CH3OH)/n(CO)增大的有
a.升高温度 b.使用催化剂 C.再充入2mol H2 d.再充入2mol He.
考点:物质的量或浓度随时间的变化曲线,化学平衡的影响因素
专题:化学平衡专题
分析:(1)由表中数据可知,开始CO的物质的量为1mol,故CO的起始浓度为
=0.5mol/L,Z的起始浓度为0,7min时反应到达平衡,平衡时CO的物质的量为0.55mol,故CO的平衡浓度为
=0.275mol/L,平衡时Z的物质的量为0.45mol,故Z的平衡浓度为
=0.225mol/L,据此作图;
(2)由表中数据可知,7min时反应到达平衡,平衡时CO的物质的量为0.55mol,H2的物质的量为0.1mol,平衡时Z的物质的量为0.45mol,计算各物质的物质的量变化量,根据物质的量变化量之比等于化学计量数之比计算各物质的量化学计量数,再利用原子守恒判断Z的分子式,据此书写;
(3)由表中数据可知3-5min时间内产物Z的物质的量变化量为0.35mol-0.25mol=0.1mol,根据v=
计算v(Z);
(4)反应物能量大于生成物能量,则反应为放热反应,如果反应物能量小于生成物能量,则反应为吸热反应;
(5)恒容条件下,使n(CH3OH)/n(CO)增大,说明平衡向正反应方向移动,可以采取的措施有:降低温度、增大氢气浓度.
| 1mol |
| 2L |
| 0.55mol |
| 2L |
| 0.45mol |
| 2L |
(2)由表中数据可知,7min时反应到达平衡,平衡时CO的物质的量为0.55mol,H2的物质的量为0.1mol,平衡时Z的物质的量为0.45mol,计算各物质的物质的量变化量,根据物质的量变化量之比等于化学计量数之比计算各物质的量化学计量数,再利用原子守恒判断Z的分子式,据此书写;
(3)由表中数据可知3-5min时间内产物Z的物质的量变化量为0.35mol-0.25mol=0.1mol,根据v=
| ||
| △t |
(4)反应物能量大于生成物能量,则反应为放热反应,如果反应物能量小于生成物能量,则反应为吸热反应;
(5)恒容条件下,使n(CH3OH)/n(CO)增大,说明平衡向正反应方向移动,可以采取的措施有:降低温度、增大氢气浓度.
解答:
解:(1)由表中数据可知,开始CO的物质的量为1mol,故CO的起始浓度为
=0.5mol/L,Z的起始浓度为0,7min时反应到达平衡,平衡时CO的物质的量为0.55mol,故CO的平衡浓度为
=0.275mol/L,平衡时Z的物质的量为0.45mol,故Z的平衡浓度为
=0.225mol/L,故CO、Z的物质的量的浓度(c)随时间(t)变化的曲线为:
 ,
,
故答案为: ;
;
(2)由表中数据可知,7min时反应到达平衡,平衡时CO的物质的量为0.55mol,故△n(CO)=1mol-0.55mol=0.45mol,H2的物质的量为0.1mol,故n(H2)=1mol-0.1mol=0.9mol,平衡时Z的物质的量为0.45mol,故CO、H2、Z的化学计量数之比为0.45mol:0.9mol:0.45mol=1:2:1,即CO+2H2=Z,故Z的分子式为CH4O,结构式为CH3OH,故该反应为CO+2H2?CH3OH,
故答案为:CO+2H2?CH3OH;
(3)由表中数据可知3-5min时间内产物Z的物质的量变化量为0.35mol-0.25mol=0.1mol,
故v(Z)=
=0.025 mol/(L?min),
故答案为:0.025 mol/(L?min);
(4)根据图象知,反应物能量大于生成物能量,则反应的正反应为放热反应,△H=419kJ/mol-510kJ/mol=-91kJ/mol,
故答案为:放热;CO(g)+2H2(g)
CH3OH(g)△H=-91kJ/mol;
(5)a.升高温度平衡向逆反应方向移动,则n(CH3OH)/n(CO)减小,故错误;
b.使用催化剂,不改变平衡移动,则 n(CH3OH)/n(CO)不变,故错误;
C.再充入2mol H2,平衡向正反应方向移动,n(CH3OH)/n(CO)增大,故正确;
d.再充入2mol He,反应物和生成物浓度不变,则平衡不移动,故错误;
故选c.
| 1mol |
| 2L |
| 0.55mol |
| 2L |
| 0.45mol |
| 2L |
 ,
,故答案为:
 ;
;(2)由表中数据可知,7min时反应到达平衡,平衡时CO的物质的量为0.55mol,故△n(CO)=1mol-0.55mol=0.45mol,H2的物质的量为0.1mol,故n(H2)=1mol-0.1mol=0.9mol,平衡时Z的物质的量为0.45mol,故CO、H2、Z的化学计量数之比为0.45mol:0.9mol:0.45mol=1:2:1,即CO+2H2=Z,故Z的分子式为CH4O,结构式为CH3OH,故该反应为CO+2H2?CH3OH,
故答案为:CO+2H2?CH3OH;
(3)由表中数据可知3-5min时间内产物Z的物质的量变化量为0.35mol-0.25mol=0.1mol,
故v(Z)=
| ||
| 5min-3min |
故答案为:0.025 mol/(L?min);
(4)根据图象知,反应物能量大于生成物能量,则反应的正反应为放热反应,△H=419kJ/mol-510kJ/mol=-91kJ/mol,
故答案为:放热;CO(g)+2H2(g)
| ||
(5)a.升高温度平衡向逆反应方向移动,则n(CH3OH)/n(CO)减小,故错误;
b.使用催化剂,不改变平衡移动,则 n(CH3OH)/n(CO)不变,故错误;
C.再充入2mol H2,平衡向正反应方向移动,n(CH3OH)/n(CO)增大,故正确;
d.再充入2mol He,反应物和生成物浓度不变,则平衡不移动,故错误;
故选c.
点评:考查反应速率计算、化学平衡有关计算、浓度随时间变化图象等,难度中等,注意作图中起点与平衡点的浓度、到达平衡的时间,(5)题d选项中,充入稀有气体,虽然容器压强增大,但反应物和生成物分压不变,反应物和生成物浓度不变,则该反应不移动,很多同学往往认为增大压强平衡向正反应方向移动而导致错误,为易错点.

练习册系列答案
相关题目
若NA代表阿伏加德罗常数,下列说法正确的是( )
| A、13g乙炔和苯的混合液中总原子数为2NA |
| B、4℃时9mL水和11.2L氮气含有相同的分子数 |
| C、同温同压下,NA个NO2与NA个N2和O2的混合气体的体积不相等 |
| D、1.01×105Pa时,11.2 L氧气所含的原子数目为NA |
分类法是一种行之有效、简单易行的科学方法.下列关于K2CO3的分类不正确的是( )
| A、钾盐 | B、有机物 |
| C、化合物 | D、碳酸盐 |
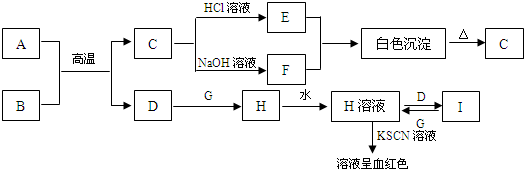
 在如图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,F在D中燃烧发出苍白色火焰.H可用于制造光导纤维,J是一种乳白色凝胶状沉淀.(部分生成物和部分反应条件未列出)
在如图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,F在D中燃烧发出苍白色火焰.H可用于制造光导纤维,J是一种乳白色凝胶状沉淀.(部分生成物和部分反应条件未列出)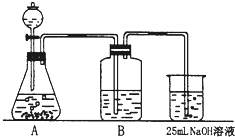 Na2CO3是一种很重要的化学物质,某学生拟在实验室中制备.下面是他的实验过程.用50mL NaOH溶液吸收CO2气体制备Na2CO3.为了防止通入的CO2过量而生成NaHCO3,他设计了如下步骤:
Na2CO3是一种很重要的化学物质,某学生拟在实验室中制备.下面是他的实验过程.用50mL NaOH溶液吸收CO2气体制备Na2CO3.为了防止通入的CO2过量而生成NaHCO3,他设计了如下步骤: