题目内容
在高温、高压和催化剂条件下的密闭容器中,进行反应:N2(g)+3H2(g)?2NH3(g)(正反应放热).下列有关说法不正确的是( )
| A、使用催化剂是为了增大化学反应速率 |
| B、增大氢气的浓度可增大反应速率 |
| C、在上述条件下,氢气能全部转化为氨气 |
| D、达到平衡时,体系中各物质的浓度不再改变 |
考点:化学反应速率的影响因素,化学平衡状态的判断
专题:化学平衡专题
分析:对于可逆反应,反应物不可能全部转化为生成物,在反应中,加入催化剂、增大反应物浓度都可增大反应速率,达到平衡状态时,正逆反应速率相等,各物质的浓度不变,以此解答.
解答:
解:A.加入催化剂,降低反应的活化能,增大活化分子的百分数,可增大反应速率,故A正确;
B.增大氢气的浓度,单位体积活化分子数目增多,反应速率增大,故B正确;
C.该反应为可逆反应,反应物不可能全部转化为生成物,故C错误;
D.达到平衡状态时,正逆反应速率相等,各物质的浓度不变,故D正确.
故选C.
B.增大氢气的浓度,单位体积活化分子数目增多,反应速率增大,故B正确;
C.该反应为可逆反应,反应物不可能全部转化为生成物,故C错误;
D.达到平衡状态时,正逆反应速率相等,各物质的浓度不变,故D正确.
故选C.
点评:本题考查化学反应速率的影响以及化学平衡状态的判断等问题,为高考常见题型和高频考点,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,注意把握可逆反应的特点,难度不大.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
近年赤潮时有发生,赤潮发生时,海水中的某些微小生物大量繁殖,使水体呈红.紫等色,并对生物造成危害,下列说法有误的是( )
| A、赤潮是水体富营养化结果 |
| B、含磷洗衣粉广泛使用与排放是发生赤潮的原因之一 |
| C、封闭的海湾更易发生 |
| D、赤潮的发生是与人类活动无关的自然现象 |
用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、28 g N2中含有氮原子数为NA |
| B、1 mol Na与足量O2反应转移的电子数为NA |
| C、常温常压下,22.4LCO2中含有的分子数为NA |
| D、1 mol?L-1K2SO4溶液中含有的钾离子数为NA |
分类法是一种行之有效、简单易行的科学方法.下列关于K2CO3的分类不正确的是( )
| A、钾盐 | B、有机物 |
| C、化合物 | D、碳酸盐 |
下列装置中能构成原电池的是( )
A、 稀硫酸 |
B、 稀硫酸 |
C、 稀硫酸 |
D、 酒精溶液 |
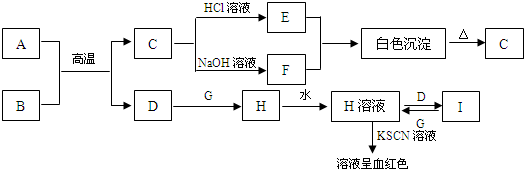
 在如图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,F在D中燃烧发出苍白色火焰.H可用于制造光导纤维,J是一种乳白色凝胶状沉淀.(部分生成物和部分反应条件未列出)
在如图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,F在D中燃烧发出苍白色火焰.H可用于制造光导纤维,J是一种乳白色凝胶状沉淀.(部分生成物和部分反应条件未列出)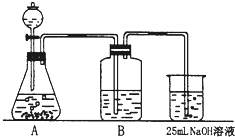 Na2CO3是一种很重要的化学物质,某学生拟在实验室中制备.下面是他的实验过程.用50mL NaOH溶液吸收CO2气体制备Na2CO3.为了防止通入的CO2过量而生成NaHCO3,他设计了如下步骤:
Na2CO3是一种很重要的化学物质,某学生拟在实验室中制备.下面是他的实验过程.用50mL NaOH溶液吸收CO2气体制备Na2CO3.为了防止通入的CO2过量而生成NaHCO3,他设计了如下步骤: