题目内容
5. 在含有弱电解质的溶液中,往往有多个化学平衡共存
在含有弱电解质的溶液中,往往有多个化学平衡共存(1)常温下,将0.2mol/L的某一元酸HA溶液和0.1mol/LNaOH溶液等体积混合后溶液pH大于7,若混合液体积等于两溶液体积之和,则混合溶液中下列关系正确的是D
A.c(HA)<c(A-)
B.c(HA)一定大于0.1mol/L
C.c(Na+)=c(HA)+c(A-)
D.2c(OH-)=2c(H+)+[c(HA)-c(A-)]
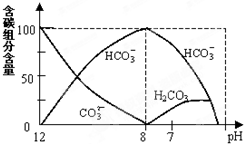
(2)常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液40mL,溶液中含碳元素的各种微粒(CO2逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示.回答下列问题:
①在同一溶液中,H2CO3、HCO3-、CO32-(填:“能”或“不能”)不能大量共存.
②当pH=7时,溶液中各种离子其物质的量浓度的大小关系是:c(Na+)>c(Cl-)>c(HCO3-)>c(H+)=c(OH-)>c(CO32-).
③已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh=$\frac{c(HC{{O}_{3}}^{-})•c(O{H}^{-})}{c(C{{O}_{3}}^{2-})}$=2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=10.
分析 (1)常温下,将0.2mol/L的某一元酸HA溶液和0.1mol/L NaOH溶液等体积混合后,得到溶液溶质为NaA和HA,溶液pH大于7,说明A-离子水解程度大于HA电离程度;
(2)常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,先反应生成碳酸氢钠,再与盐酸反应生成二氧化碳、水,以此分析解答.
解答 解:(1)0.2mol/L的某一元酸HA溶液和0.1mol/L NaOH溶液等体积混合后,反应后得到等量的HA、NaA,溶液pH大于7,则盐类水解大于酸的电离,
A. 水解生成HA,则c(HA)>c(A-),故A错误;
B.因等体积混合,则反应后c(HA)一定小于0.1mol/L,故B错误;
C.反应后得到等量的HA、NaA,则2c(Na+)=c(HA)+c(A-),故C错误;
D.由电荷守恒可知,c(Na+)+c(H+)=c(OH-)+c(A-),又2c(Na+)=c(HA)+c(A-),则c(OH-)=c(H+)+$\frac{1}{2}$[c(HA)-c(A-)],故D正确;
故答案为:D;
(2)常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,先反应生成碳酸氢钠,再与盐酸反应生成二氧化碳、水,
①由反应及图象可知,在同一溶液中,H2CO3、HCO3-、CO32-不能大量共存,故答案为:不能;
②当pH=7时,溶液中溶质为碳酸氢钠、氯化钠,离子浓度大小为:c(Na+)>c(Cl-)>c(HCO3-)>c(H+)=c(OH-)>c(CO32-);
故答案为:c(Na+)>c(Cl-)>c(HCO3-)>c(H+)=c(OH-)>c(CO32-);
③水解常数Kh=$\frac{c(HC{{O}_{3}}^{-})•c(O{H}^{-})}{c(C{{O}_{3}}^{2-})}$=2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,c(OH-)=10-4mol/L,由Kw可知,c(H+)=10-10mol/L,所以pH=10,
故答案为:10.
点评 本题考查较综合,涉及溶液中离子浓度大小分析,化学平衡常数的计算及溶液中酸碱之间的反应,题目难度较大,综合考查学生分析问题、解决问题的能力,注重能力的考查.

 阅读快车系列答案
阅读快车系列答案| A. | CH3COOH溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO?) | |
| B. | 常温下,pH=2的CH3COOH溶液与pH=12的NaOH 溶液等体积混合后溶液的pH=7 | |
| C. | CH3COOH溶液中加入少量CH3COONa固体.平衡逆向移动 | |
| D. | 室温下向pH=3的醋酸溶液中加水稀释,溶液中$\frac{[C{H}_{3}CO{O}^{-}]}{[C{H}_{3}COOH][O{H}^{-}]}$不变 |
| A. | 某吸热反应能自发进行,因此该反应是熵增反应 | |
| B. | 加入NaHCO3使氯水的漂白能力增强 | |
| C. | 难溶电解质可以由溶解度小的转化为溶解度更小的,但不能从溶解度小的转化为溶解度大的 | |
| D. | Ksp只受温度的影响,不受浓度的影响 |
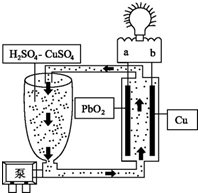 流动电池是一种新型电池.其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定.我国某研究小组新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4═CuSO4+PbSO4+2H2O.下列说法不正确的是( )
流动电池是一种新型电池.其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定.我国某研究小组新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4═CuSO4+PbSO4+2H2O.下列说法不正确的是( )| A. | a为正极,b为负极 | |
| B. | 该电池工作时PbO2电极附近溶液的pH增大 | |
| C. | b极的电极反应为Cu-2e-═Cu2+ | |
| D. | 调节电解质溶液的方法是补充CuSO4 |
| A. | 18O只存在于乙酸分子中 | |
| B. | 18O存在于乙酸和乙酸乙酯中分子中 | |
| C. | 18O只存在于乙醇分子中 | |
| D. | 18O存在于水、乙酸分子中 |
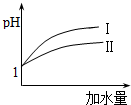 已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+△H>0.
已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+△H>0.
 CH3COOCH2CH3+H2O,酯化反应或取代反应.
CH3COOCH2CH3+H2O,酯化反应或取代反应.