题目内容
15.将乙醇、浓硫酸和乙酸混合,加热一段时间,再加入少量H218O,充分反应.下列说法中正确的是( )| A. | 18O只存在于乙酸分子中 | |
| B. | 18O存在于乙酸和乙酸乙酯中分子中 | |
| C. | 18O只存在于乙醇分子中 | |
| D. | 18O存在于水、乙酸分子中 |
分析 乙醇与乙酸发生酯化反应时,乙酸提供羧基中的羟基,乙醇提供羟基上的氢原子,结合生成水,剩余基团结合生成乙酸乙酯,酯化反应是可逆反应,以此来解答.
解答 解:乙醇与乙酸发生酯化反应时,乙酸提供羧基中的羟基,乙醇提供羟基上的氢原子,结合生成水,剩余基团结合生成乙酸乙酯,而酯化反应是可逆反应,则加入H218O加热一段时间后,18O存在于H218O、乙酸中,
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握酯化反应中化学键的断裂及可逆反应特点为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
3.对于100mL 0.5mol/LH2SO4溶液与铁片的反应,采取下列措施能使反应速率加快的是:①升高温度;②改用100mL 1.0mol/LH2SO4溶液;③改用300mL 0.5mol/LH2SO4溶液;④用等量铁粉代替铁片;⑤改用质量分数为98%的H2SO4溶液( )
| A. | ①③④ | B. | ①②④ | C. | ①②③④ | D. | ①②③⑤ |
7.某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的方程式中不合理的是(已知:饱和NaClO溶液的pH约为11)( )
| A. | 该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-→ClO-+Cl-+H2O | |
| B. | 该消毒液的pH约为12:ClO-+H2O?HClO+OH- | |
| C. | 该消毒液与洁厕灵(主要成分为HCl)混用,产生有毒Cl2:2H++Cl-+ClO-→Cl2↑+H2O | |
| D. | 该消毒液加白醋生成HClO,可增强漂白作用:H++ClO-→HClO |
4.下列关于能量转化的认识不正确的是( )
| A. | 原电池工作时,化学能转化为电能 | |
| B. | 手机电池在充电时,是电能转变为化学能 | |
| C. | 煤燃烧时,化学能主要转化为热能 | |
| D. | 人体运动所消耗的能量与化学反应无关 |
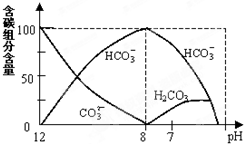 在含有弱电解质的溶液中,往往有多个化学平衡共存
在含有弱电解质的溶液中,往往有多个化学平衡共存