题目内容
3.(1)常见的氨基酸结构简式:甘氨酸的为:H2NCH2COOH,丙氨酸为: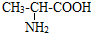 .
.(2)氨基酸的分子中既含有氨基,又含有羧基,既能和酸反应又能和_碱反应生成盐.
分析 (1)甘氨酸是氨基乙酸;丙氨酸是α氨基丙酸,据此解题;
(2)氨基酸是至少包含一个氨基和一个羧基的化合物,氨基酸既是酸又是碱,与酸或者碱都能反应生成盐,它们具有两性,据此解题.
解答 解:(1)甘氨酸结构简式:H2NCH2COOH;丙氨酸的结构简式为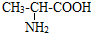 ;
;
故答案为:H2NCH2COOH;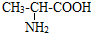 ;
;
(2)氨基酸是至少包含一个氨基和一个羧基的化合物,氨基酸既是酸又是碱,与酸或者碱都能反应生成盐,它们具有两性;
故答案为:氨基;羧基;酸;碱.
点评 本题考查常见氨基酸的结构简式、氨基酸的结构和性质特点,题目难度不大,注意基础知识的积累,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
14.下列反应中水只作还股剂的是( )
| A. | 2H2O$\frac{\underline{\;通电\;}}{\;}$ 2H2↑+O2 | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | Cl2+H2O═HC1+HC1O | D. | 2F2+2H2O═4HF+O2 |
8.下列说法正确的是( )
| A. | 增大压强,活化分子数增加,化学反应速率一定增大 | |
| B. | 升高温度,活化分子百分数增加,化学反应速率一定增大 | |
| C. | 加入反应物,使活化分子百分数增加,化学反应速率增大 | |
| D. | 使用催化剂,降低了反应的活化能、反应速率加快,但是活化分子百分数不变 |
15.对下列金属采取的防护方法中,属于电化学防护的是( )
| A. | 在轮船水线以下的船体装上一定数量的锌块 | |
| B. | 在金属表面进行电镀 | |
| C. | 在一定条件下对金属进行处理,在其表面形成一层致密的氧化膜 | |
| D. | 将铁闸门与直流电源的正极相连 |
 某化学活动小组设计实验(装置如图)验证氯、溴、碘及其化合物的有关物质.在硬质玻璃管中的A、B、C三处依次放置湿润的蓝色石蕊试纸、浸有NaBr溶液的棉球、浸有淀粉-KI溶液的棉球(如图所示),由左端通入足量氯气,回答下列问题:
某化学活动小组设计实验(装置如图)验证氯、溴、碘及其化合物的有关物质.在硬质玻璃管中的A、B、C三处依次放置湿润的蓝色石蕊试纸、浸有NaBr溶液的棉球、浸有淀粉-KI溶液的棉球(如图所示),由左端通入足量氯气,回答下列问题: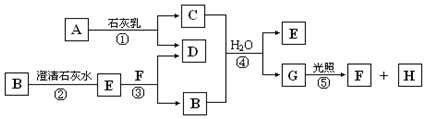 图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如图转化关系(反应中生成的水已略去).
图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如图转化关系(反应中生成的水已略去).