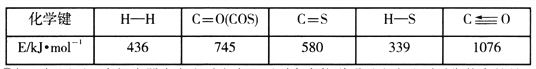
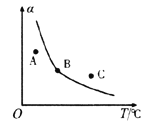
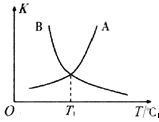
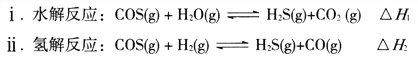��Ŀ����
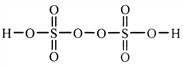
����Ŀ��ijһ��Ӧ��ϵ���з�Ӧ��������ﹲ�������ʣ�O2��H2CrO4��Cr(OH)3��H2O��H2O2����֪�÷�Ӧ��H2O2ֻ�������¹��̣�H2O2��O2��
(1)�÷�Ӧ�еĻ�ԭ����____________��
(2)�÷�Ӧ�У�������ԭ��Ӧ�Ĺ�����______________��______________��
(3)д���÷�Ӧ�Ļ�ѧ����ʽ������˫���ŷ��������ת�Ƶķ������Ŀ��__________��
(4)����Ӧת����0.3 mol���ӣ�������������ڱ�״�������Ϊ__________L��
���𰸡�H2O2 H2CrO4Cr(OH)3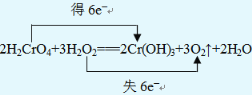 3.36
3.36
��������
��1������ϢH2O2��O2�п�֪��OԪ�صĻ��ϼ���-1�����ߵ�0����H2O2Ϊ��ԭ�����������������������H2O2��
��2��������������ԭ��Ӧ������Ԫ�ػ��ϼ۽��͵�����Ϊ����������CrԪ�صĻ��ϼ۽��ͣ�����ԭ��Ӧ�Ĺ���ΪH2CrO4��Cr��OH��3���������������������� H2CrO4��Cr��OH��3��
��3����Ӧ��H2O2�е�OԪ��ʧ���ӣ�H2CrO4�е�CrԪ�صõ����ӣ�2molH2CrO4��Ӧת�Ƶ���Ϊ2mol����6-3��=6mol������˫���ŷ��������ת�Ƶķ������ĿΪ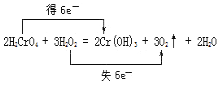 ����������������������
���������������������� 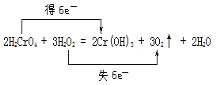 ��
��
��4����2H2CrO4+3H2O2�T2Cr��OH��3��+3O2��+2H2O ��Ӧ��֪������3mol����ת��6mol���ӣ���ת����0.3mol���ӣ����������������ʵ���Ϊ0.3/6��3mol=0.15mol�����ڱ�״�������Ϊ0.15mol��22.4L/mol=3.36L�������������������ǣ�3.36L��

 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�����Ŀ�����й�Ҫǿ���й���������Ҫ�ã�������ǿ��Ƽ������ҹ������ش�Ƽ��л� ŵ���������ǣ� ��
A | B | C | D |
|
|
|
|
����������DZˮ�� ʵ��ɹ� | �״��˹��� �ɽᾧ ţ�ȵ��� | ��°������� �Ƽ | ���������ƿ�ű��ҩ-������ |
A. A B. B C. C D. D
����Ŀ�����������ȷ���ǣ� ��
ѡ�� | ���� | �� | �� | ���� |
A | ˮ�� | ���� | ���� | ��������Һ |
B | ��ˮ | ���� | �ռ� | �� |
C | C60 | ���� | ��ʯ�� | �� |
D | ���� | ̼�� | ������ͭ | ������������ |
A.AB.BC.CD.D