题目内容
写出下列情况所发生的化学反应方程式:
(1)向NaHCO3溶液中滴入:
①少量Ca(OH)2溶液 ;
②过量Ca(OH)2溶液 ;
(2)向10mL 1mol/L的NH4HCO3溶液中逐滴滴入:
①2mL 3mol/L的NaOH溶液 ;
②20mL 1mol/L的NaOH溶液 .
(1)向NaHCO3溶液中滴入:
①少量Ca(OH)2溶液
②过量Ca(OH)2溶液
(2)向10mL 1mol/L的NH4HCO3溶液中逐滴滴入:
①2mL 3mol/L的NaOH溶液
②20mL 1mol/L的NaOH溶液
考点:化学方程式的书写
专题:元素及其化合物
分析:(1)①向NaHCO3溶液中滴入少量Ca(OH)2溶液,生成碳酸钙和碳酸钠;
②向NaHCO3溶液中滴入过量Ca(OH)2溶液,生成碳酸钙和氢氧化钠;
(2)向10mL 1mol/L的NH4HCO3溶液中逐滴滴入NaOH溶液,氢氧化钠先和HCO3-反应,再和NH4+反应.
②向NaHCO3溶液中滴入过量Ca(OH)2溶液,生成碳酸钙和氢氧化钠;
(2)向10mL 1mol/L的NH4HCO3溶液中逐滴滴入NaOH溶液,氢氧化钠先和HCO3-反应,再和NH4+反应.
解答:
解:(1)①向NaHCO3溶液中滴入少量Ca(OH)2溶液,生成碳酸钙和碳酸钠,方程式为2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O,
故答案为:2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O;
②向NaHCO3溶液中滴入过量Ca(OH)2溶液,生成碳酸钙和氢氧化钠,方程式为NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O,
故答案为:NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O;
(2)①向10mL 1mol/L的NH4HCO3溶液中逐滴滴入2mL 3mol/L的NaOH溶液,n(NH4HCO3):n(NaOH)=5:3,氢氧化钠先和HCO3-反应,
则发生2NH4HCO3+2NaOH=(NH4)2CO3+Na2CO3+2H2O,
故答案为:2NH4HCO3+2NaOH=(NH4)2CO3+Na2CO3+2H2O;
②向10mL 1mol/L的NH4HCO3溶液中逐滴滴入20mL 1mol/L的NaOH溶液,n(NH4HCO3):n(NaOH)=1:2,完全反应,
发生NH4HCO3+2NaOH=Na2CO3+H2O+NH3?H2O,
故答案为:NH4HCO3+2NaOH=Na2CO3+H2O+NH3?H2O.
故答案为:2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O;
②向NaHCO3溶液中滴入过量Ca(OH)2溶液,生成碳酸钙和氢氧化钠,方程式为NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O,
故答案为:NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O;
(2)①向10mL 1mol/L的NH4HCO3溶液中逐滴滴入2mL 3mol/L的NaOH溶液,n(NH4HCO3):n(NaOH)=5:3,氢氧化钠先和HCO3-反应,
则发生2NH4HCO3+2NaOH=(NH4)2CO3+Na2CO3+2H2O,
故答案为:2NH4HCO3+2NaOH=(NH4)2CO3+Na2CO3+2H2O;
②向10mL 1mol/L的NH4HCO3溶液中逐滴滴入20mL 1mol/L的NaOH溶液,n(NH4HCO3):n(NaOH)=1:2,完全反应,
发生NH4HCO3+2NaOH=Na2CO3+H2O+NH3?H2O,
故答案为:NH4HCO3+2NaOH=Na2CO3+H2O+NH3?H2O.
点评:本题考查化学方程式的书写,为高频考点,侧重于学生的分析能力的考查,本题侧重于与量有关的化学方程式的书写,注意把握反应的程度,难度中等.

练习册系列答案
相关题目
去除氧化膜的镁条插入盛有少量饱和FeCl3溶液的试管中,片刻后大量反应液涌向试管中,反应液呈现深红棕色,并有大量的红褐色固体物质,取出镁条、冲洗,发现镁条表面完全变黑,靠近磁铁,镁条立即被吸起来.依据上述实验现象的推论不正确的是( )
| A、Fe3+比H+的氧化性强,故镁将Fe3+还原完全后再与H+反应 |
| B、镁和生成的铁构成许多微型原电池,故反应剧烈 |
| C、反应放热温度升高,故反应剧烈 |
| D、反应产物含有Fe(OH)3、Fe、H2 |
下列描述正确的是( )
| A、氯气、活性炭都能使品红溶液褪色,它们的漂白原理相同 |
| B、滴加石蕊试液显红色的溶液:Fe3+、NH4+、I-可能大量共存 |
| C、某溶液中加入盐酸酸化的氯化钡产生白色沉淀,原溶液中一定含有SO42- |
| D、Fe(N03)2溶液中滴加少量稀硫酸会变黄色 |
 现有FeCl3、FeCl2、CuCl2的混合溶液1L,将0.70mol的铁粉慢慢加入混合液中并充分搅拌,溶液中的三种金属阳离子的物质的量随铁粉加入量的变化曲线如图所示,D点坐标是(0.4,0),H点坐标是(0.7,0.2).
现有FeCl3、FeCl2、CuCl2的混合溶液1L,将0.70mol的铁粉慢慢加入混合液中并充分搅拌,溶液中的三种金属阳离子的物质的量随铁粉加入量的变化曲线如图所示,D点坐标是(0.4,0),H点坐标是(0.7,0.2).
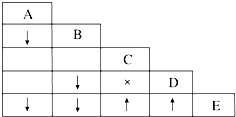 有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、BaCl2溶液、K2CO3溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各取少量,多次进行两两混合反应,反应现象如表所示.表中“↓”表示生成沉淀,“↑”表示生成气体,“×”表示没有明显现象,空格表示实验未做.
有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、BaCl2溶液、K2CO3溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各取少量,多次进行两两混合反应,反应现象如表所示.表中“↓”表示生成沉淀,“↑”表示生成气体,“×”表示没有明显现象,空格表示实验未做.