题目内容
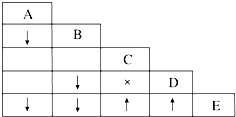 有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、BaCl2溶液、K2CO3溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各取少量,多次进行两两混合反应,反应现象如表所示.表中“↓”表示生成沉淀,“↑”表示生成气体,“×”表示没有明显现象,空格表示实验未做.
有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、BaCl2溶液、K2CO3溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各取少量,多次进行两两混合反应,反应现象如表所示.表中“↓”表示生成沉淀,“↑”表示生成气体,“×”表示没有明显现象,空格表示实验未做.请回答下列问题:
(1)各试剂瓶中所盛试剂为(填溶质的化学式)
A
(2)写出下列反应的离子方程式.
A与E:
B与E:
C与E:
考点:物质的检验和鉴别的实验方案设计
专题:实验设计题
分析:C与E、D与E产生气体,五种物质中,能与两种物质的产生气体的只有K2CO3,则E为K2CO3,则C、D为HNO3、HCl中的物质,而D与B能产生沉淀,则D为HCl,能与硝酸银产生AgCl沉淀,所以C为HNO3,B为AgNO3,则A为BaCl2,结合物质的性质,可写出反应的离子方程式.
解答:
解:(1)C与E、D与E产生气体,五种物质中,能与两种物质的产生气体的只有K2CO3,则E为K2CO3,则C、D为HNO3、HCl中的物质,而D与B能产生沉淀,则D为HCl,能与硝酸银产生AgCl沉淀,所以C为HNO3,B为AgNO3,则A为BaCl2,
故答案为:BaCl2;AgNO3;HNO3;HCl;K2CO3;
(2)A为BaCl2,E为K2CO3,二者反应生成BaCO3,反应的离子方程式为Ba2++CO32-=BaCO3↓,
B为AgNO3,E为K2CO3,二者反应生成Ag2CO3,反应的离子方程式为2Ag++CO32-=Ag2CO3↓,
C为HNO3,E为K2CO3,二者反应生成CO2,反应的离子方程式为2H++CO32-=CO2↑+H2O,
故答案为:Ba2++CO32-=BaCO3↓;2Ag++CO32-=Ag2CO3↓;2H++CO32-=CO2↑+H2O.
故答案为:BaCl2;AgNO3;HNO3;HCl;K2CO3;
(2)A为BaCl2,E为K2CO3,二者反应生成BaCO3,反应的离子方程式为Ba2++CO32-=BaCO3↓,
B为AgNO3,E为K2CO3,二者反应生成Ag2CO3,反应的离子方程式为2Ag++CO32-=Ag2CO3↓,
C为HNO3,E为K2CO3,二者反应生成CO2,反应的离子方程式为2H++CO32-=CO2↑+H2O,
故答案为:Ba2++CO32-=BaCO3↓;2Ag++CO32-=Ag2CO3↓;2H++CO32-=CO2↑+H2O.
点评:本题考查物质的检验和鉴别,为高频考点,把握发生的反应及习题中的信息为解答的关键,侧重分析、推断能力的考查,注意E为碳酸钾为推断的突破口,题目难度不大.

练习册系列答案
相关题目
下列图示实验正确的是( )
A、 碳酸氢钠受热分解 |
B、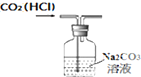 除去CO2中HCl |
C、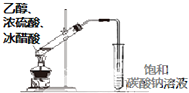 制备乙酸乙酯 |
D、 制备收集干燥的氨气 |
下列关于漂白粉的叙述正确的是( )
| A、漂白粉的有效成分是Ca(ClO)2和CaCl2 |
| B、漂白粉在空气中久置后会变质 |
| C、漂白粉的有效成分CaCl2 |
| D、漂白粉的主要成分是CaCl2 |
下列物质不能用于鉴别碳酸钠溶液和碳酸氢钠溶液的是( )
| A、稀盐酸 | B、氯化钙溶液 |
| C、澄清石灰水 | D、稀硫酸 |
