题目内容
下列判断正确的是( )
| A、等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、C、Si和Ge的最外层电子数都是4,次外层电子数都是8 |
| C、若A2+2D-=2A-+D2,则氧化性:A2>D2 |
| D、CO2和SiO2都是酸性氧化物,都不能和氧化钙反应 |
考点:硅和二氧化硅,氧化性、还原性强弱的比较
专题:氧化还原反应专题,碳族元素
分析:A.同一物质,气态时能量大于固态时能量,根据能量守恒判断;
B.C原子次外层电子数是2、Ge次外层电子数是18;
C.自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
D.高温下,二氧化硅和氧化钙反应生成硅酸钙.
B.C原子次外层电子数是2、Ge次外层电子数是18;
C.自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
D.高温下,二氧化硅和氧化钙反应生成硅酸钙.
解答:
解:A.同一物质,气态时能量大于固态时能量,根据能量守恒知,等质量的硫蒸气和硫固体分别完全燃烧,前者放出热量多,故A错误;
B.C原子次外层电子数是2,Si、Ge次外层电子数是18,Si次外层电子数是8,故B错误;
C.该反应中氧化剂是A2、氧化产物是D2,所以氧化性A2>D2,故C正确;
D.高温下,二氧化硅和氧化钙反应生成硅酸钙,反应方程式为SiO2+CaO
CaSiO3,故D错误;
故选C.
B.C原子次外层电子数是2,Si、Ge次外层电子数是18,Si次外层电子数是8,故B错误;
C.该反应中氧化剂是A2、氧化产物是D2,所以氧化性A2>D2,故C正确;
D.高温下,二氧化硅和氧化钙反应生成硅酸钙,反应方程式为SiO2+CaO
| ||
故选C.
点评:本题考查较综合,涉及物质之间反应、氧化性强弱比较、原子结构、能量守恒等知识点,根据物质的性质、氧化性强弱比较、原子结构分析解答,知道能量越低的物质越稳定.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
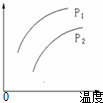 在容积一定的密闭容器中发生可逆反应A(g)+2B(g)?2C(g)-Q,条件变化时,影响平衡移动的关系如图所示.下列说法正确的是( )
在容积一定的密闭容器中发生可逆反应A(g)+2B(g)?2C(g)-Q,条件变化时,影响平衡移动的关系如图所示.下列说法正确的是( )| A、P1<P2,纵坐标指A的质量分数 |
| B、P1>P2,纵坐标指C的质量分数 |
| C、P1<P2,纵坐标指混合气体的平均摩尔质量 |
| D、P1>P2,纵坐标指A的转化率 |
下列离子方程式中正确的是( )
| A、Al(OH)3滴加稀盐酸:OH-+H+=H2O |
| B、Fe片浸泡在FeCl3溶液中:Fe3++Fe=2Fe2+ |
| C、MgCl2溶液中滴加氨水:Mg2++2OH-=Mg(OH)2↓ |
| D、NaHSO4溶液中加BaCl2溶液:SO42-+Ba2+=BaSO4↓ |
下列关于原电池的叙述中错误的是( )
| A、在原电池中,电子流出的一极是负极,发生氧化反应 |
| B、原电池是将化学能转变为电能的装置 |
| C、构成原电池的正极和负极必须是两种不同的金属 |
| D、原电池放电时,在外电路电子的流动方向是从负极到正极 |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、42.0 g乙烯和丙烯的混合气体中含有的碳原子数为3NA |
| B、常温常压下,17g甲基(-14CH3)所含的中子数为9NA |
| C、标准状况下,11.2L苯中含有的碳碳双键数为1.5NA |
| D、1mol氯气与氢氧化钙溶液完全反应生成氯化钙和氯酸钙,转移的电子数为6NA |
分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法.下列关于NaHCO3的分类正确的是( )
| A、酸 | B、氧化物 | C、有机物 | D、钠盐 |